时间:2017-01-13 09:10:11
1、实验题 (4分)用50 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)烧杯间填满碎泡沫塑料的作用是???????????????????????????????????????????????????????????;
(2)实验时氢氧化钠溶液的浓度要用0.55 mol/L的原因是?????????????????????????????????????????????????????????????????????;实验中若改用60 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的氢氧化钠溶液进行反应,与上述实验相比,所放出的热量????(填“相等”或“不相等”),若实验操作均正确,则所求中和热???????(填“相等”或“不相等”);
参考答案:(1)减少热量损失(1分)
(2)为了确保盐酸完全被中
本题解析:略
本题难度:简单
2、简答题 某课外小组设计如图1所示装置进行探究实验(夹持装置已略去).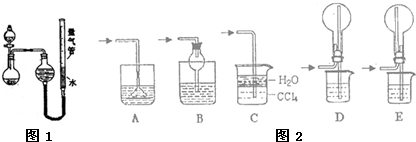
(1)实验过程中,使用分液漏斗滴加液体的操作是______.
(2)利用该装置抽取氨气并测量其体积,请回答下列有关问题.
①反应前,烧瓶中可加入的试剂是______,量气装置中的液体最好换用______(填字母编号).
a.稀NaOH溶液;b.CaO;c.煤油;d.氯化铵溶液;e.NaOH固体;f.氨水.
②该实验剩余的NH3需吸收处理.如图2所示的各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有______(填字母编号).
③本实验就对量气管多次读数,读数时应注意:Ⅰ.将实验装置恢复到室温;Ⅱ.______;Ⅲ.视线与凹液面最低处相平.
(3)该小组同学欲利用NH3、CO2和NaC1溶液模拟工业制碱,则在饱和NaC1溶液中通入气体的顺序依次为______,其反应的化学方程式为______.
(4)某同学认为利用上述所设计的装置也可进行铜与稀硝酸的反应,通过收集并测量NO气体的体积以测定铜的纯度.你认为______(填“可行”或“不可行”),理由是______.
参考答案:(1)分液漏斗用于气体发生器中控制加液,也常用于互不相溶的几
本题解析:
本题难度:一般
3、简答题 下表是甲城市某日空气质量报告:
| 城市 | 污染指数 | 首要污染物 | 空气质量级别 | 空气质量状况 甲 55 SO2 Ⅱ 良 该市某校研究性学习小组对表中首要污染物SO2导致酸雨的成因进行探究. 【探究实验】 实验一:用如图所示装置进行实验. 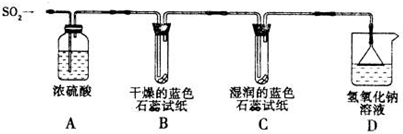 ①A装置的作用是______(填“干燥”或“氧化”)SO2气体. ②实验过程中,B装置内石蕊试纸的颜色没有发生变化,C装置内湿润的蓝色石蕊试纸变______色,说明SO2与水反应生成一种酸,该酸的化学式是______. ③D装置的作用是______.若实验中向装置内通入标准状况下1.12LSO2气体,且NaOH溶液过量.最多能生成Na2SO3的物质的量为______mol.(反应的化学方程式为:SO2+2NaOH=Na2SO3+H2O) 实验二:往盛有水的烧杯中通入SO2气体,测得所得溶液的pH______7(填“>”、“=”或“<”=,然后每隔1h测定其pH,发现pH逐渐变小,直至恒定.说明烧杯中溶液被空气中的氧气氧化最终生成H2SO4. 【查阅资料】 SO2形成酸雨的另一途径;SO2与空气中的O2在飘尘的作用下反应生成SO3,SO3溶于降水生成H2SO4.在此过程中飘尘作 【探究结论】 SO2与空气中的氧气、水反应生成硫酸而形成酸雨.本市可能易出现酸雨, 【知识联想】 (1)酸雨造成的危害是:______(举一例). (2)汽车排放的尾气,硝酸、化肥等工业生产排出的废气中都含有氮的氧化物,氮的氧化物溶于水最终转化为______,是造成酸雨的另一主要原因. 【提出建议】 本市汽车数量剧增,为了减少汽车尾气造成的污染,建议市政府推广使用混合型汽油,即往汽油中按一定比例加入______(填“水”或“乙醇”). 参考答案:实验一:①二氧化硫与浓硫酸不反应,浓硫酸有吸水性,可以吸收二 本题解析: 本题难度:一般 4、选择题 下列有关实验操作、现象和解释或结论都正确的是 (????? )
|