溶液的pH
①
22.00
0
8
②
22.00
18.00
7
③
22.00
22.00
6
假设溶液混合前后的体积变化忽略不计,则c为( )
A.3
B.4
C.5
D.6
2、填空题 (1)体积相同、浓度均为0.2mol/L的盐酸和醋酸溶液分别加水稀释10倍,溶液的pH分别变成m和n,则m和n的关系是________,稀释后两溶液中和NaOH的能力_______。??
(2)25℃时,pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合,混合后溶液呈_____(填“酸性”“碱性”或“中性”), 混合后溶液中离子浓度由大到小的顺序是_______________________。??
(3)25℃时,将Va mLpH=1的硫酸溶液与Vb mLpH=12的氢氧化钾溶液混合恰好呈中性,则Va:Vb=________。
3、选择题 已知温度T时水的离子积常数为KW,该温度下,将浓度为amol?L-1的一元酸HA与bmol?L-1一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A.a=b
B.混合溶液的pH=7
C.混合溶液中,c(H+)= Kw
mol?L-1
D.混合溶液中,c(H+)+c(B-)=c(OH-)+c(A-)
4、选择题 25℃时,将pH=a的CH3COOH溶液VamL与pH=12的NaOH溶液VbmL混合.下列说法正确的是( )
A.若Va=Vb,且NaOH与CH3COOH恰好完全反应,则a>2
B.若a=2,混合后溶液pH=7,则混合后V总>2Vb
C.若a=2,混合后溶液pH<7,则Va一定大于Vb
D.若Va=Vb,a=2,混合液中微粒浓度关系为:c(Na+)>c(CH3COO-)>c(OH-)>c( H+)
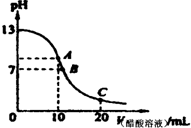
5、选择题 25℃时,在20mL?0.1mol/L NaOH溶液中逐滴加入0.2mol/L醋酸溶液,曲线如图所示,
有关粒子浓度关系的比较中,不正确的是( ) A.在A点:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
B.在B点:c(OH-)═c(H+),c(Na+)═c(CH3COO-)
C.在C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D.在C点:c(CH3COO-)+c(CH3COOH)═2c(Na+)
微信搜索关注"91考试网"公众号,领30元,获取公务员事业编教师考试资料40G
|
|