时间:2017-01-13 08:35:33
1、实验题 22、某研究小组按图示方向将A装置与下面所示装置相连,设计实验,研究铁与浓硫酸的反应。请你帮助完成下列实验报告,并回答有关问题。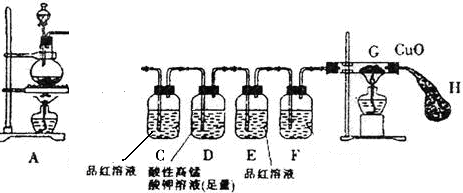
| 实验现象 | 结论及解释 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ①将铁钉(足量)加入烧瓶中,再向其中滴加含amolH2SO4的浓硫酸溶液 | 未见明显现象 | 原因: ???????????????????。 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ②点燃A、G处酒精灯 | 片刻后,烧瓶中溶液的颜色发生变化,并有气泡产生。C中溶液颜色??????,E中溶液未见明显变化。一段时间后,黑色的CuO变成了红色,此时E装置溶液颜色仍未有颜色变化 | 烧瓶中发生的所有反应 的化学方程式: ????????????????????????? ????????????????????????? 说明产生的SO2气体完全被D中溶液吸收 填完上述实验报告并回答下列问题: (1)连接好装置后,盛放药品前,首先要进行??????????????????????操作。 (2)装置D的作用是?????????????????????????,若现在实验室没有酸性高锰酸钾溶液,则D装置中的溶液可用??????????(填编号)代替 A、蒸馏水?????? B、浓硫酸?????? C、浓NaOH溶液???? D、饱和NaHSO3溶液 (3)装置F中的溶液是???????????????,装置H的作用是:???????????????????????????????????? (4)为了测定产生的SO2的量,实验后向烧瓶中加足量的盐酸至无气泡产生,再加足量的BaCl2溶液至沉淀完全,然后进行???????????、?????????????、干燥、称量。为判断沉淀完全,应该进行的操作是:??????????????????????????????????????????????????。 (5)若(4)所得沉淀的质量为mg,则反应产生的SO2在标准状况的体积为: ???????????????????????????L(列出计算式即可) 2、选择题 下列说法不正确的是[???? ] 3、选择题 通过量CO2于下列溶液中,出现浑浊的是( ) 4、实验题 (13分)I.某校化学实验小组探究浓度对化学反应速率的影响,并测定(NH4)2S2O8和KI反应的化学反应速率。进行如下实验探究:
(3)第①组实验的v(S2O82-)=????????????????????mol・(L・s)-1。 (4)根据上表数据分析,可以得到的结论有(写出一条即可)????????????????????? ???????????????????????????????????????????????????????????????????????????。 II.实验小组查资料得知,向含有Na2CO3的Na2S溶液中通入SO2,可以制备上述实验所需的Na2S2O3。反应如下:Na2CO3 + SO2= Na2SO3 + CO2;2Na2S + 3SO2 = 2Na2SO3 + 3S↓; Na2SO3 + S= Na2S2O3。该小组根据上述原理设计下图所示装置制备Na2S2O3。  (1)实验应避免有害气体排放到空气中。装置①、②中盛放的试剂依次是 ①????????????????????????????????; ②????????????????????????????????。 (2)实验过程中,随着气体的通入,装置①中有气泡产生,还有大量黄色固体析出,继续通入气体,可以观察到的现象是?????????????????????????????????????????????。 (3)反应结束后,从制得的Na2S2O3稀溶液中得到Na2S2O3・5H2O晶体的主要操作包括:???????????????????????????????????????????????????????????????????。 5、实验题 铁生锈是比较常见的现象,某实验小组,为研究铁生锈的条件,设计了以下快速、易行的方法: | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||