时间:2017-01-12 17:54:46
1、选择题 下列物质含有离子键的是( )
A.Cl2
B.NaCl
C.CO2
D.H2O
2、选择题 下列说法正确的是( )
A.C和Si属于第ⅣA族元素,C非金属性比Si强,CO2、SiO2均是酸性氧化物
B.Na2O2与水反应,红热的Fe与水蒸气反应均能生成碱
C.NaHCO3、Na2CO3两种固体分别加热后均有气体生成
D.氮、硫的单质及其氢化物在一定条件下均可与氧气反应,都直接生成NO2、SO2
3、选择题 下 列化学式及结构式中成键情况不合理的是[???? ]
A. CH3N 
B. CH2SeO 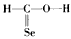
C. CH4S 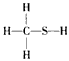
D. CH4Si 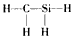
4、选择题 下列化学用语正确的是( )
A.氮分子的电子式: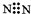
B.硫原子的结构示意图: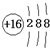
C.溴化钠的电子式: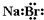
D.水分子的结构式: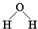
5、填空题 (16分)A、B、C是中学化学中常见的三种短周期元素。已知:①A元素原子最外层电子数是次外层电子数的2倍;②B元素最高正价与最低负价的代数和为2;③C元素有多种化合价,且常温下C元素的单质与某种一元强碱溶液反应,可得到两种含C元素的化合物;④B、C两种元素质子数之和是A元素质子数的4倍。
(1) 写出A元素在周期表中的位置_______________________。
(2) 写出C的单质和强碱溶液反应的离子方程式____________________________________。
(3) 意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的B4气态分子。B4分子结构与白磷分子结构相似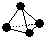 ,已知断裂1 mol B―B吸收167 kJ的热量,生成1 mol B≡B放出942 kJ热量。试写出由B4气态分子变成B2气态分子的热化学方程式:____________________________。
,已知断裂1 mol B―B吸收167 kJ的热量,生成1 mol B≡B放出942 kJ热量。试写出由B4气态分子变成B2气态分子的热化学方程式:____________________________。
(4) 由B、C两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X分子为三角锥形
分子,且分子里B、C两种原子最外层均达到8个电子的稳定结构。X遇水蒸气可形成一种常见的漂白性物质。则X的结构式为____________,X与水反应的化学方程式是___________________。
(5) A、B两种元素可形成一种硬度比金刚石还大的化合物Y。在化合物Y中,A、B原子间以单键相结合,且每个原子的最外层均达到8个电子的稳定结构。则Y的化学式为______________,Y晶体的熔点比金刚石熔点______(填“高”或“低”)。
(6) B2H4是一种可燃性液体,其水溶液呈弱碱性,是因为溶液中存在平衡:
H2B-BH2+H2O _________________________。
_________________________。