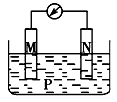
参考答案:当闭合开关K时,b附近溶液先变红,即b附近有氢氧根生成,所以在b极上得电子析出氢气,b极是阴极,a极是阳极,与阴极连接的是原电池的负极,所以B极是负极,A极是正极.
A、闭合K时,负极发生氧化反应,电极反应为2Na2S2-2e-=2Na++Na2S4,故A错误;
B、闭合K时,有0.01molNa+通过离子交换膜,说明有0.01mol电子转移,阴极上生成0.005molH2,标准状况下体积为0.005mol×22.4L/mol=0.112L=112?mL,故B正确;
C、闭合开关K时,b极附近先变红色,该极上是氢离子放电的过程,即b附近有氢氧根生成,pH增大,故C错误;
D、闭合开关K时,a极是阳极,该极上金属铜电极是活泼电极,发生的电极反应为:Cu-2e-=Cu2+,没有气体产生,故D错误.
故选B.
M
?N
P
A.
锌?
铜
稀硫酸溶液
B.
铜?
铁
稀盐酸
C.
银?
锌
硝酸银溶液
D.
锌?
铁
硝酸铁溶液
参考答案:C
本题解析:
本题难度:简单
3、选择题 固体电解质是通过离子迁移传递电荷。如RbAg4I5晶体,其中迁移的物种全是Ag+,利用RbAg4I5晶体,可以制成电化学气敏传感器,下图是一种测定O2含量的气体传感器示意图。被分析的O2可以透过聚四氟乙烯薄膜,由电池电动势变化可以得知O2的含量。在气体传感器工作过程中,下列变化肯定没有发生的是(?)

A.Ag-e-=Ag+
B.I2+2Ag++2e-=2AgI
C.I2+2Rb++2e-=2RbI
D.4AlI3+3O2=2Al2O3+6I2
参考答案:C
本题解析:由图可知,传感器中发生4AlI3+3O2=2Al2O3+6I2,原电池的负极发生Ag-e-=Ag+,正极发生I2+2Ag++2e-=2AgI,所以肯定没有的反应是I2+2Rb++2e-=2RbI,答案选C。
本题难度:简单
4、填空题 (5)现有A、B、C、D四种金属片,①把A、B用导线连接后同时浸入稀硫酸溶液中,A上有气泡产生;②把C、D用导线连接后同时浸入稀硫酸溶液中,D发生还原反应;③把A、C用导线连接后同时浸入稀硫酸溶液中,电子流动方向为A→导线→C。根绝上述情况,回答下列问题:
(1)在①中,金属片?发生氧化反应
(2)在②中,金属片?作负极
(3)如果把B、D用导线连接后同时浸入稀硫酸溶液,则金属片?上有气泡产生
(4)上述四种金属的活动顺序是?
参考答案:.(1) B?(2)C?(3)D?(4)B>A>C>D
(3)PbSO4+2e-=Pb+SO42-;PbSO4+2H2O-2e-= PbO2+4H++ SO42-
本题解析:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。
(1)把A、B用导线连接后同时浸入稀硫酸溶液中,A上有气泡产生,说明A是正极,B是负极,所以金属B发生氧化反应,因此金属性是B大于A。
(2)把C、D用导线连接后同时浸入稀硫酸溶液中,D发生还原反应,说明D是正极,C是负极,所以金属性是C大于D。
(3)A、C用导线连接后同时浸入稀硫酸溶液中,电子流动方向为A→导线→C,所以金属性是A大于C,所以金属性强弱顺序为B>A>C>D。因此如果把B、D用导线连接后同时浸入稀硫酸溶液,则B是负极,D是正极,溶液中的氢离子在正极得到电子,生成氢气。
本题难度:一般
5、填空题 (17分)铜在工农业生产中有着广泛的用途。
(1)配制CuSO4溶液时需加入少量稀H2SO4,其原因是 (只写离子方程式)。
(2)某同学利用制得的CuSO4溶液,进行以下实验探究。
①图甲是根据反应Fe+CuSO4=Cu+FeSO4设计成铁铜原电池,请图甲中的横线上完成标注。

②图乙中,I是甲烷燃料电池的示意图,该同学想在II中实现铁上镀铜,则应在a处通入 (填“CH4”或“O2”),b处电极上发生的电极反应式为 ==4OH-;
若把II中电极均换为惰性电极,电解液换为含有0.1molNaCl溶液400mL,当阳极产生的气体为448mL(标准状况下)时,溶液的pH= (假设溶液体积变化忽略不计)。
(3)电池生产工业废水中常含有毒的Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去[室温下Ksp(FeS)=6.3×10-18mol2・L-2,Ksp(CuS)=1.3×10-36mol2・L-2]。请结合离子方程式说明上述除杂的原理:当把FeS加入工业废水中后,直至FeS全部转化为CuS沉淀,从而除去溶液中Cu2+。
参考答案:(1)Cu2++2H2O Cu(OH)2+2H+
Cu(OH)2+2H+
(2)①(见图)
②CH4 O2+4e-+2H2O 13
(3)存在溶解平衡:FeS(s) Fe 2+(aq)+ S 2-(aq),其中的Cu2+与S 2-生成了溶度积更小的CuS沉淀,使得上述溶解平衡继续向右移动。[或用平衡FeS(s)+Cu2+(aq)=" CuS(s)+" Fe 2+(aq)解释]
Fe 2+(aq)+ S 2-(aq),其中的Cu2+与S 2-生成了溶度积更小的CuS沉淀,使得上述溶解平衡继续向右移动。[或用平衡FeS(s)+Cu2+(aq)=" CuS(s)+" Fe 2+(aq)解释]
本题解析:(1)加入稀硫酸是为了抑制Cu2+的水解;(2)图乙在Fe上镀铜,所以Fe作阴极,则连接的为燃料电池的负极,应通入CH4,b极通入O2发生还原反应:O2+4e-+2H2O =4OH-;电解池中均为惰性电极时,阳极的电极反应式为:2Cl--2e-=Cl2↑ ,阴极反应式为:2H++2e-=H2 ↑ .由电极反应式计算消耗的H+为0.04mol,则生成的OH-为0.04mol,c(OH-)=0.1mol/L,则c(H+)=10-13mol/L,pH=13;(3)应用了难溶电解质的沉淀溶解平衡,溶液中存在溶解平衡:FeS(s)  Fe 2+(aq)+ S 2-(aq),Cu2+与S 2-反应可生成溶度积更小的CuS沉淀,使得上述溶解平衡继续向右移动。
Fe 2+(aq)+ S 2-(aq),Cu2+与S 2-反应可生成溶度积更小的CuS沉淀,使得上述溶解平衡继续向右移动。
考点:盐类水解、原电池原理及计算、难溶电解质的沉淀溶解平衡。
本题难度:困难