时间:2025-06-26 02:35:44
1、选择题 下表是元素周期表的一部分。X、Y、Z、W均为短周期元素,Z元素原子的最外层电子数与电子总数之比为3:8。则下列说 法中正确的是 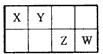
[? ]
A.四种元素中Z的非金属性最强
B.X元素只能形成一种单质
C.Y元素可形成多种氧化物
D.四种元素的最高价氧化物对应的水化物都是强酸
2、选择题 下表是X、Y、Z三种元素单质的某些性质

[? ]
3、选择题 下列具有特殊性能的材料中,由主族元素和副族元素形成的化合物是( )
A.半导体材料砷化镓
B.吸氢材料镧镍合金
C.透明陶瓷材料硒化锌
D.超导材K3C60
4、选择题 下列各组元素性质递变情况错误的是
[? ]
A.Li、Be、B原子最外层电子数依次增多
B.P、S、Cl元素最高正化合价依次升高
C.N、P、F原子半径依次增大
D.Na、K、Rb的金属性依次增强
5、选择题 下列各组物质中互为同位素的是
[? ]
A.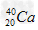 和
和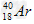 ?
?
B.D和T?
C.H2O和H2O2?
D.O3和O2?