时间:2025-06-26 01:59:56
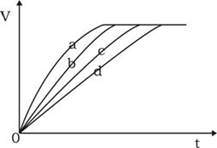
1、选择题 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积v的数据,根据数据绘制得到下图,则曲线a所对应的实验组别是
| 组别 | ?c(HCl)? mol/L | 温度(℃) | 状态 |
| A | 2.0 | 25 | 块状 |
| B | 2.5 | 30 | 块状 |
| C | 2.5 | 50 | 粉末 |
| D | 2.5 | 50 | 块状 |
参考答案:C
本题解析:根据图像可知,a对应的曲线斜率最大,说明反应速率最快。由于升高温度、增大反应物浓度或增大反应物的接触面积都是加快反应速率的,所以答案选C。
本题难度:简单
2、选择题 下列实验中,反应速率加快是由催化剂引起的是( )
A.在炭粉中加入KCl03,点燃时燃烧更为剧烈
B.将炭块粉碎成粉末状,可使燃烧更加充分
C.H2O2中加入少量MnO2,即可迅速放出气体
D.电解水时,加少量硫酸可使电解速率加快
参考答案:A.在炭粉中加入氯酸钾,氯酸钾分解生成氧气,促进燃烧,点燃时燃烧更为剧烈,与催化剂无关,故A错误;
B.炭块粉碎成粉末状,固体表面积增大,反应速率增大,与催化剂无关,故B错误;
C.在双氧水的分解反应中,二氧化锰起到催化剂的作用,故C正确;
D.用锌与稀硫酸反应制备氢气时,加入少量浓硫酸,氢离子浓度增大,反应速率增大,与催化剂无关,故D错误.
故选C.
本题解析:
本题难度:简单
3、填空题 在400 ℃、101 kPa时,NO2(g)+CO(g)==NO(g) + CO2(g)反应过程的能量变化如下图所示。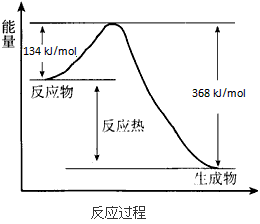
(1)该反应是________(填“吸热”或“放热”)反应。
(2)该反应的热化学方程式为________________。
(3)改变下列条件都可使该反应的反应速率改变,其中通过降低活化能加快反应速率的是_______。
a.浓度 b.压强 c.温度 d.催化剂
参考答案:(1)放热
(2)NO2(g)+CO(g)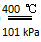 NO(g) + CO2(g) ΔH=-234 kJ/mol
NO(g) + CO2(g) ΔH=-234 kJ/mol
(3)d
本题解析:
本题难度:一般
4、选择题 下列说法正确的是
[? ]
参考答案:C
本题解析:
本题难度:一般
5、填空题 (8分)某学生为了探究锌与盐酸反应过程中的速率变化,他在100 mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值,且气体体积为标况体积):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
参考答案:①2-3min?反应放热,温度升高,反应速率加快
②0.1mol/(L・min)? ③AB
本题解析:(1)在0~1、1~2、2~3、3~4、4~5min时间段中,产生气体的体积分别是:50 mL、 70mL 、112mL、68mL、20 mL,由此知反应速率最大的时间段为2-3min;反应速率刚开始增大后来又逐渐减小与反应物的浓度无关,只能是与反应的热效应有关。
(2)在2~3分钟时间段内,n(H2)= 0.112L/22.4L/moL=0.005mol,则消耗盐酸的物质的量=2n(H2),则υ(HCl)=0.1mol/(L・min)。
(3)A、加入蒸馏水,H+浓度减小,反应速率减小但不减少氢气的量,正确;B、加入NaCl溶液,H+浓度减小,反应速率减小但不减少氢气的量,正确;C、加入NaNO3溶液,生成NO气体,影响生成氢气的量,错误;D、加入CuSO4溶液,Zn置换出Cu形成原电池,使反应速率增大,但影响生成氢气的量,错误;E、加入Na2CO3溶液,消耗H+而使H+浓度减小,影响生成氢气的量,错误。
本题难度:一般