时间:2025-06-26 01:59:56
1、简答题 化学在环境保护中起着十分重要的作用.催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染.
(1)催化反硝化法中,H2能将NO3-还原为N2.25℃时,反应进行l0min,溶液的pH由7变为12.
①N2的结构式为______.
②上述反应的离子方程式为______,其平均反应速率v(NO3-)为______mol?L-1?min-1.
③还原过程中可生成中间产物NO2-,写出2种促进NO2-水解的方法
______.
(2)电化学降解NO3-的原理如图所示.
①电源正极为______(填“A”或“B”),阴极反应式为:______.
②若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差______(△m左-△m右)为g.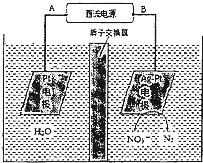
2、选择题 在相同条件下(T=500k),相同体积甲、乙两容器,甲充入1gSO2、1gO2,乙充入2gSO2、2gO2.下列叙述错误的是
A.化学反应速率乙>甲
B.平衡后O2浓度乙>甲
C.SO2转化率乙>甲
D.平衡后SO2的体积分数乙>甲
3、简答题 (15分)某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4 + 5H2C2O4 + 3H2SO4= K2SO4 + 2MnSO4 + 10CO2↑ + 8H2O
【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量 / mL | 室温下溶液颜色褪至无色所需时间 / min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 3 mol/L 稀硫酸 | 0.05mol/L KMnO4溶液 | ||
| 1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
| 2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
| 3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |

| 实验编号 | 室温下,试管中所加试剂及其用量 / mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间 / min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 3 mol/L 稀硫酸 | 0.05 mol/L KMnO4溶液 | |||
| 4 | 3.0 | 2.0 | 2.0 | 3.0 | | t |
4、填空题 氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率v(纵坐标)与反应时间t(横坐标)的关系如图所示,已知该反应速率随着溶液中c(H+)的增大而加快。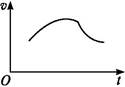
(1)反应开始时反应速率加快的原因是
(2)反应后期反应速率减慢的原因是 。?
5、选择题 已知?4NH3(气)+5O2(气)=4NO(气)+6H2O(气),若反应速率分别是V(NH3)、V(O2)、V(NO)、V(H2O)[mol/L?min]表示,则正确的关系是( )
A.
| 4 5 |
| 5 6 |
| 3 2 |
| 5 4 |