时间:2025-06-26 01:33:46
1、选择题 甲、乙两容器都发生反应2 A(g)+B(g) 3C(g),两容器温度和初始压强都相同。在甲恒容容器中充入2 mol A和1 mol B,达平衡后,C在平衡混合气中的体积分数为φ1、物质的量为n1;在乙恒压容器中充入1.4 mol A、0.7 mol B和0.6 mol C,达平衡后C在平衡混合气中的体积分数为φ2、物质的量为n2。下列说法中正确的是(?)
3C(g),两容器温度和初始压强都相同。在甲恒容容器中充入2 mol A和1 mol B,达平衡后,C在平衡混合气中的体积分数为φ1、物质的量为n1;在乙恒压容器中充入1.4 mol A、0.7 mol B和0.6 mol C,达平衡后C在平衡混合气中的体积分数为φ2、物质的量为n2。下列说法中正确的是(?)
A.φ1>φ2? B.n1>n2?C.n1=n2? D.φ1<φ2
参考答案:B
本题解析:因为若X=3则恒压或恒容条件都一样,只要符合比例就等效,达平衡后C在平衡混合气中的体积分数相等,则A、D错误;由于两容器的“初始压强”相同,即初始体积不一样,开始时两容器体积比为物质的量之比3:2.7=10∶9,即此时乙比甲投料总物质的量少(乙容器相当于充入1.8 mol A和0.9 mol B),所以达平衡时n1>n2,则C错误,B正确。
本题难度:一般
2、选择题 下列事实不能用勒沙特列原理解释的是( )
A.合成氨反应:N2(g)+3H2(g)
2NH3(g);△H<0,为使氨的产率提高,理论上应采取低温高压的措施
B.对2HI(g)
H2(g)+I2(g)平衡体系增加压强使颜色变深
C.使用催化剂有利于提高SO2与O2生成SO3的效率
D.用排饱和氯化钠溶液的方法来收集氯气
参考答案:A.对N2(g)+3H2(g)
2NH3(g);△H<0,正反应为气体总物质的量减小的反应,且正反应为放热反应,为使氨的产率提高,就要使化学平衡向正反应方向移动,就要降温并且加压,A与勒夏特列原理符合,故A错误;
B.对2HI(g)
H2(g)+I2(g)反应前后气体的总物质的量相等,增大压强,平衡不移动,气体颜色变深是因为体积减小,I2的物质的量浓度增大,不能用勒夏特列原理解释,故B正确;
C.催化剂只能同等程度地改变正逆反应速率,对化学平衡无影响,即不能用勒夏特列原理解释,故C正确;
D.排饱和氯化钠溶液的方法来收集氯气,相当于对Cl2+H2O?H++Cl-+HClO加入NaCl,增大了Cl-的难度,使平衡向逆反应方向移动,降低了氯气的溶解度,即可用勒夏特列原理解释,故D错误;
故选BC.
本题解析:
本题难度:简单
3、选择题
对达到平衡状态的可逆反应:A+B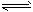 C+D ,若t1时增大压强,正、逆反应速率变化如图所示(ν代表反应速率,t代表时间),下列有关A、B、C、D的状态叙述中正确的是
C+D ,若t1时增大压强,正、逆反应速率变化如图所示(ν代表反应速率,t代表时间),下列有关A、B、C、D的状态叙述中正确的是
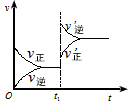
参考答案:C
本题解析:
本题难度:一般
4、填空题 空气质量与我们的健康息息相关,目前我国通过监测6项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2和CO是其中3项中的污染物。
(1)上述3种气体直接排入空气后会引起酸雨的气体有 (填化学式)。
(2)早期人们曾经使用铅室法生产硫酸,其主要反应为:
SO2(g)+NO2(g) SO3(g)+NO(g)
SO3(g)+NO(g)
①若已知2SO2(g)+O2(g) 2SO3(g) ΔH=a kJ・mol-1
2SO3(g) ΔH=a kJ・mol-1
2NO(g)+O2(g) 2NO2(g) ΔH=b kJ・mol-1
2NO2(g) ΔH=b kJ・mol-1
则SO2(g)+NO2(g) SO3(g)+NO(g) ΔH= kJ・mol-1。
SO3(g)+NO(g) ΔH= kJ・mol-1。
②一定温度下,向固定体积为2 L的密闭容器中充入SO2和NO2各1 mol,发生反应:SO2(g)+NO2(g) SO3(g)+NO(g)。下列事实中不能说明该反应达到平衡状态的是 (选填序号)。
SO3(g)+NO(g)。下列事实中不能说明该反应达到平衡状态的是 (选填序号)。
a.体系压强保持不变 b.混合气体的颜色保持不变
c.NO的物质的量保持不变 d.每生成1 mol SO3的同时消耗1 mol NO2
③测得②中反应5 min末到达平衡,此时容器中NO与NO2的体积比为3
参考答案:
本题解析:
本题难度:困难
5、选择题 已知反应A2(g)+2B2(g)?2AB2(g)(正反应放热),下列说法正确的( )
A.升高温度,正向反应速率减小,逆向反应速率增加
B.升高温度有利于反应速率增加,从而缩短达到平衡的时间
C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
参考答案:解;A、升高温度,正向反应速率、逆向反应速率均增加,故A错误;
B、升高温度有利于反应速率增加,从而缩短达到平衡的时间,故B正确;
C、达到平衡后,升高温度,平衡向着逆向进行,增大压强平衡正向移动,故C错误;
D、达到平衡后,降低温度或增大压强都有利于该反应平衡正向移动,故D错误.
故选B.
本题解析:
本题难度:简单