时间:2025-06-26 01:30:30
1、选择题 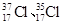 为不同的核素,
为不同的核素,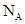 为阿伏加德罗常数,下列说法正确的是
为阿伏加德罗常数,下列说法正确的是
A.常温下,4.48L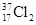 含有0.72
含有0.72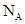 个中子
个中子
B.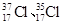 互为同位素,
互为同位素,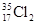 与
与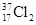 互为同分异构体
互为同分异构体
C.通常情况下,氯气做氧化剂,但氯气也具有还原性
D.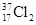 的摩尔质量是74
的摩尔质量是74
2、选择题 我国科学家最近发现一种只有六个中子构成的粒子,这种粒子称为“六中子”,也有人称之为“零号元素”。下列有关“六中子”粒子的说法不正确的是
A.该粒子不显电性
B.该粒子质量数为6
C.在周期表中与氢元素占同一位置
D.该粒子质量比氢原子的大
3、选择题 下列各组物质的比较,不正确的是( ?)
A.碱性:NaOH>Mg(OH)2>Al(OH)3
B.热稳定性:HCl>HBr>HI
C.原子序数:Cl>S>P
D.原子半径:F>O>N
4、选择题 表示一个原子的M电子层上有10个电子,可以写成(? )
A.3s23p63d2
B.3d10
C.3s23p64s2
D.3s23p33d5
5、选择题 下图是某短周期元素最高价氧化物对应水化物相同浓度稀溶液的pH与原子半径的关系示意图,则下列说法正确的是(双选) ( )。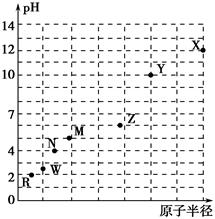
A.原子序数:W>Z>X
B.气态氢化物的稳定性:N>R
C.Y和W形成共价化合物
D.X、Z的最高价氧化物对应的水化物能相互反应