时间:2025-06-26 01:30:30
1、填空题 (5分)在原子结构理论中,有四个原理,分别是①构造原理,②泡利原理,③洪特规则,④能量最低原理。在以下的现象中主要决定的因素是(填序号,各只填一项)
(1)各能级最多容纳的电子数是该能级原子轨道数的2倍?;
(2)碳原子的核外电子排布基态时是1s22s22p2而不是1s22s12p3?;
(3)最外层电子数不会超过8个,次外层电子数不会超过18个?;
(4)铬(24Cr)的电子排布式是1s22s22p63s23p63d54s1而不是1s22s22p63s23p63d44s2?;
(5)磷原子的基态原子结构中,有3个未成对的单电子?。
2、填空题 Al和Ga及N和As分别是同主族的元素,请回答下列问题:
(1)砷化镓是一种半导体材料,其化学式为?。
(2)写出As原子处于基态时的核外电子排布式?。
(3)超高导热绝缘耐高温纳米氮化铝在绝缘材料中应用广泛,氮化铝晶体与金刚石类似,每个铝原子与?个氮原子相连,氮化铝晶体属于?晶体。
(4)NH3是氮的氢化物,中心原子的杂化方式是?,存在化学键的类型是?,NH3的沸点比AsH3高的原因是?。
3、选择题 下列各组物质的熔点变化规律,与它们的化学键无关的是
A.F2、Cl2、Br2、I2的熔点依次升高
B.Li、Na、K、Rb的熔点依次降低
C.NaF、NaCl、NaBr、NaI的熔点依次降低
D.晶体硅、碳化硅、金刚石的熔点依次升高
4、填空题 (15分)A、B、C、D、E、F、G、H八种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B、C、D为同一周期,A与E,B与G,D与H分别为同一主族,C和D的最外层电子数之和为11,C、D、F三种元素的原子序数之和为28。请回答下列问题:
(1)B与D可形成非极性分子X,X的结构式为?。
(2)E、F、H所形成的简单离子的半径由大到小的顺序为(用离子符号表示)?。
(3)G的最高价氧化物与B的单质在高温下能发生置换反应,其化学反应方程式为:
?。
(4)盐Y由B、D、E组成。以熔融盐Y为电解质构成的燃料电池如图所示。写出石墨(I)电极上发生的电极反应式:?。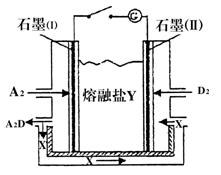
(5)用熔融盐Y的燃料电池作电源,以石墨为电极,电解一定浓度的CuSO4溶液至无色后继续电解一段时间。断开电路,向溶液中加入0.1 mol Cu(OH)2,溶液恢复到电解之前的体积和浓度,则电解过程中转移电子的物质的量为______。
(6)由A、C、D、E四种元素中任意三种构成的强电解质Z和W,溶于水时都能促进水的电离,测得Z的水溶液pH>7,W的水溶液pH<7,则Z为??、W为?。
5、填空题 A、B、C、D、E五种元素均为短周期元素,原子序数逐渐增大。A形成的单质密度最小(相同条件下)。B可形成多种同素异形体,其中一种的硬度自然界中最大。D元素原子的最外层电子数是次外层电子数的3倍。E元素的最高价氧化物的水化物的酸性强于硫酸。
(1)元素C位于元素周期表的?周期?族,原子结构示意图为?。
(2)B、C、D三种元素的最简单氢化物的稳定性从大到小的顺序是?(填化学式),BE4分子的空间构型是?。
(3)元素A与B形成原子个数比为1:1的相对分子质量最小的化合物的结构式为?。
(4)A、B、C、D几种元素之间可以形成多种10电子微粒,写出上述10电子微粒之间反应的其中一个化学方程式或离子方程式:?
(5)写出E的单质制取漂白粉反应的化学方程式并标出电子转移的方向和数目:?