ʱ��:2025-06-26 01:26:27
1��ѡ���� ����ˮ�еμ���ɫʯ���Լ�����������������ȷ����?��?����
A����ҺѸ����Ϊ��ɫ
B����Һ��Ϊ��ɫ
C����Һ�ȱ�죬����ɫ
D����Һ����ɫ
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
2��ʵ���� ij��ȤС����Ʋ�����������ʵ����̽��Cl2��Ư�۵��Ʊ����й����ʡ�
��1��ʵ������������װ���Ʊ����﴿�����������밴������������������ķ��������������ӣ�
H�������������������������������������������������������ƿ���е��Լ�Ϊ��������������������������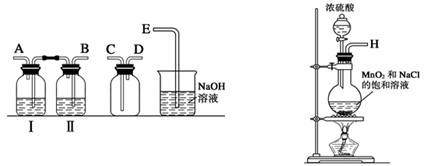
��2��д����ҵ����������ʯ������ȡƯ�۵Ļ�ѧ��Ӧ����ʽ��
������������������������������������������������������������������������������������������
ijѧ���������ʵ���һ��̽��SO2��Ư�۾��ķ�Ӧ��
| ���� | ���� |
| ȡ4 gƯ�۾����壬����100 mLˮ | ���ֹ����ܽ⣬��Һ������ɫ |
| ���ˣ���Ư�۾���Һ��pH | pH��ֽ�ȱ�����ԼΪ12��������ɫ |
 A | ��.Һ���Ϸ�������״�� ��.�Ժ��ֻ��ǣ���Һ��Ϊ����ɫ ��.�Ժ���������ɫ����������ɫ��ȥ |
 �ķ����ǣ���?����������������������������������������
�ķ����ǣ���?�����������������������������������������ο��𰸣���1��BACDE? (1��)������ʳ��ˮ(1��)
��2��2Ca(OH)2 +2 Cl2 ��Ca(ClO)2 +CaCl2 +2H2O (2��)
��3�����ԡ�Ư����? (2��)
��4���ų���������(1�֣���������)
��5����Ư�۾���Һ����μ������ᣬ�۲���Һ�Ƿ��Ϊ����ɫ(1�֣���������)
��6��SO2 +Cl2 +2H2O �� H2SO4 +2HCl? (2��)��ȡ�����������������ᱵ��������������ȡ�ϲ���ҹ��������������ϡ���ᣬ������ɫ������˵����Cl����(2��)
�����������1���Ʊ�������ʵ���У�Ҫ��ȥ�����Ȼ����ˮ�����������õ�ϴ��װ�ã�һ���dz����̳������˳��Ϊ��B A C D E������Ϊ���ȳ�ȥ������е��Ȼ��⣬��˹��ƿ���е��Լ�Ϊ����ʳ��ˮ���������ڱ���ʳ��ˮ���ܽ�Ƚ�С����
��2��д����ҵ����������ʯ������ȡƯ�۵Ļ�ѧ��Ӧ����ʽ��2Ca(OH)2 +2 Cl2 ��Ca(ClO)2 +CaCl2 +2H2O ��
��3��pH��ֽ��ɫ�ȱ���˵���ʼ��ԣ�����ɫ˵��Ư�۾���Ư���ԡ�
��4����ͬѧ�Ʋ�����i����״��������СҺ���γɣ���������ʵ����Խ�һ����֤��a����ʪ��ĵ⻯�ص�����ֽ������״��ޱ仯Ŀ�����ų��������š�
��5����������Һ��Ϊ����ɫ˵�����������ɣ�ʵ���Ǵ����������������������Һ�з����˷�Ӧ��ֻҪ���ò��������ӵ���Һ���Խ�����֤���ɣ�����Ϊ��Ư�۾���Һ����μ������ᣬ�۲���Һ�Ƿ��Ϊ����ɫ��
��6�����л���ɫ��ȥ��ԭ�Ƕ���������л�ԭ�Ժ���������������ԭ��Ӧ��SO2 +Cl2 +2H2O �� H2SO4 +2HCl��������ɫ����Һ���Ƿ��������ӵķ�����ȡ�����������������ᱵ��������������ȡ�ϲ���ҹ��������������ϡ���ᣬ������ɫ������˵����Cl����2��Ư�۵��Ʊ����й����ʡ�
�����Ѷȣ�һ��
3��ѡ���� HClO�DZ�̼�ỹ�����ᣬ��Ӧ��Cl2+H2O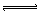 HCl+HClO��ƽ���ҪʹHClOŨ�����ӣ��ɼ���?
HCl+HClO��ƽ���ҪʹHClOŨ�����ӣ��ɼ���?
A��H2S������
B��HCl
C��CaCO3���̣�
D��H2O
�ο��𰸣�C
�������������Ҫ������������ʿ��ƻ�ԭ��ѧƽ�Ⲣ����[HClO]��Ũ�ȡ�
A��ͨ���ΪH2S�����ǻ�ԭ������HClO���������ԣ�����H2Sһ�����HClO��Ӧ����A���Ǵ𰸡���������ƽ�����淽���ƶ���Ҳ�����HClO����BҲ���Ǵ𰸡�����CaCO3��CaCO3����HCl��Ӧ��������HClO��Ӧ����Ϊ�������������ǿ������˳����HCl��H2CO3��HClO�����������ܺ�̼��Ʒ�Ӧ����HClO�����Ա�H2CO3�������Բ�����CaCO3��Ӧ������CaCO3�ɼ�СHClŨ��ƽ�����������ƶ���HClO���μӷ�Ӧ����Ũ������CΪ�𰸡�����ˮ��ѧƽ������������Ӧ�����ƶ�������ˮ����Һ��ϡ��HClOŨ��Ҳ��С��
�����Ѷȣ�һ��
4��ѡ���� ������������ȷ����
A����ˮӦ��������ɫ��ϸ���Լ�ƿ��
B��Һ��Ӧ������ĥ�ڲ�������ɫ�Լ�ƿ�У���������ˮ����ˮ��
C����ʹʪ��ĵ��۵⻯����ֽ����������һ��������
D���������ھƾ��������þƾ��ӵ�ˮ����ȡ�ⵥ��
�ο��𰸣�B
�����������
�����Ѷȣ���
5��ѡ���� ��ʮһ��ȫ�˻���ϰ���������Ӿ�ݵ�ˮ�ʴ」����Ӿ��������������Ӿ�ص�ˮ����ɰ��һ����һ����̿��ˮ���ս��д���������ɰ�ˡ�����������̿�����÷ֱ��ǣ�?��
A������������������
B��ɱ����Ư�ס�����
C�����ˡ�Ư�ס�����
D�����ˡ�����������
�ο��𰸣�D
�����������
�����Ѷȣ�һ��