时间:2025-06-26 01:25:39
1、推断题 在化合物YX2和ZX2中,已知X、Y、Z都是前三周期的元素,X与Y同周期,Y与Z同主族,Y原子的最外层电子数是次外层电子数的2倍;X原子最外层上有6个电子。根据以上条件,回答问题: ?
(1)Y的原子结构示意图为______________; ?
(2)YX2的结构式是___________,分子内的共价键是______________(填“极性键”或“非极性键”)。?
(3)ZX2的化学式为__________。 ?
(4)用电子式表示YX2的形成过程________________。
2、填空题 用短周期元素的元素符号回答以下有关问题:
(1)大气中含最多的元素是______.
(2)相对原子质量最小的元素是______.
(3)地壳中含量居首位的金属元素是______.
(4)最高价氧化物的水化物呈两性的元素是______.
3、推断题 【三选一----物质结构与性质】?
有?X、Y、Z、W四种元素,其中X是周期表中原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29。
请回答下列问题:
(1)由X、Y构成的10电子化合物的分子式为___________;基态Y原子的核外电子排布式为___________;
(2)离子Z3-的中心原子轨道杂化类型为____________,离子Z3-?的空间构型为___________;
(3)化合物ZX3的沸点比化合物YX4的高,其主要原因是____________?。
(4)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化物的分子式是______________。
(5)元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是____________,它可与浓盐酸发生非氧化还原反应,生成配合物H2WCl3,反应的化学方程式为_____________。 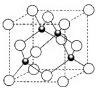
4、选择题 已知A、B、C、D、E是核电核数依次增大的五种短周期元素,原子半径按D、E、B、C、A顺序依次减小,B和E同主族,下列排列不正确的是
A.A、B、E一定不在同一周期
B.A、D可能在同一主族
C.C的最高价氧化物的水化物可能显碱性
D.C和D的单质间化合可能形成离子化合物
5、推断题 已知A、J、D、E、G是元素周期表中1~36号元素,其原子序数依次增大。A与另外四种元素既不在同一周期,也不在同一主族。J和D同主族,E和G同周期:元素G是周期表中的第7列元素,E的最外层电子数与最内层电子数相同,E跟J 可形成离子化合物,其晶胞结构(其中J原子在晶胞内部)如图。 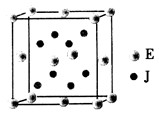
请回答下列问题:
(1)D元素-1价离子的电子排布式为________;G元素原子的价电子排布式为_________。
(2)元素J与氮元素可以形成化合物NJ3,其中N-J键的化学键类型为_____________,根据价层电子对互斥理论可以判断NJ3的空间构型为________,NJ3分子中N原子的杂化方式为________杂化。
(3)A、J形成的化合物AJ的相对分子质量比A、D形成的化合物AD的相对分子质量小,但AJ的沸点比AD 高,其原因是_____________。
(4)从晶胞图可以得出:E与J形成的离子化合物的化学式为_____________。
(5)含有E元素的化合物焰色反应为________色,焰色反应的原理是__________________。