时间:2025-06-26 01:20:45
1、选择题 在KClO3+6HCl=3Cl2↑+ KCl+3H2O中,有30 mole-转移,生成的氯气在标准状况下的体积为
A.22.4L
B.336.0L
C.403.2L
D.672.0L
参考答案:C
本题解析:根据方程式可知氯酸钾中氯元素的化合价从+5价降低到0价,得到5个电子。盐酸中氯元素的化合价从―1价升高到0价,失去1个电子,即氯气既是氧化产物,也是还原产物。每得到3mol氯气转移5mol电子,所以有30 mole-转移,得到氯气是18mol,则生成的氯气在标准状况下的体积为18mol×22.4L/mol=403.2L,答案选C。
考点:考查氧化还原反应的计算
本题难度:一般
2、选择题 判断一个反应是否为氧化还原反应的标准是
A.是否有氧参加反应
B.化合物是否分解
C.同一元素的化合价在反应前后是否发生变化
D.是否为化合或分解反应
参考答案:C
本题解析:氧化还原反应的特征是反应前后同一元素的化合价发生变化,C项正确。
本题难度:简单
3、选择题 下列各项中表达正确的是
A.H2O2的电子式:
B.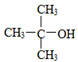 的命名:2,2―二甲基―2―乙醇
的命名:2,2―二甲基―2―乙醇
C.常温下,浓度都为0.1mol・Lˉ1的Na2CO3、NaHCO3溶液的pH,前者小于后者
D.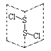 为二氯化二硫(S2Cl2)的结构,分子中有极性键、非极性键,是极性分子
为二氯化二硫(S2Cl2)的结构,分子中有极性键、非极性键,是极性分子
参考答案:D
本题解析:A 错误,H2O2是共价化合物,电子式中没有中括号
B 错误命名:2-甲基-2-丙醇
C 错误,浓度相同时,碳酸钠的碱性强于碳酸氢钠的碱性,即前者的PH大于后者。
D 正确。
本题难度:一般
4、选择题 下列过程中,不涉及氧化还原反应的是
A.浓硫酸加入蔗糖固体中
B.金属钠放置在空气中变质
C.SO2使品红溶液褪色
D.NO2形成酸雨
参考答案:C
本题解析:A.浓硫酸加入蔗糖固体中使蔗糖碳化变黑,发生了氧化还原反应
B.金属钠放置在空气中变质最终生成了碳酸钠粉末,发生了氧化还原反应
C.SO2使品红溶液褪色体现了SO2的漂白性,是化合性漂白,没发生氧化还原反应
D.NO2形成酸雨是NO2与水反应生成硝酸和NO,化合价有变化,发生了氧化还原反应
本题难度:简单
5、填空题 (4分)完成并配平下列化学方程式□FeO + □HNO3――□Fe(NO3)3 + NO↑+ □ ,
该反应中氧化剂是 ,当生成2mol NO时,转移的电子数为 NA。
参考答案: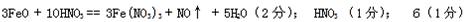
本题解析:略
本题难度:一般