ʱ��:2025-06-26 01:09:15
1������� ��6�֣�����пԭ����У�������ͭΪ�������Һ��пΪ �����缫�Ϸ�������________��Ӧ(����������ԭ��)�� ��Ϊ__ ___�����缫��Ӧʽ��___ _ _____���������Ͽɹ۲쵽��������_ _______��ԭ��ط�Ӧ�����ӷ���ʽΪ_________��
�ο��𰸣��� ������������Cu2����2e��=Cu���к�ɫ����������Zn��Cu2��=Zn2����Cu
�������������ԭ��ص�Ӧ���жϡ���ԭ����нϻ��õĽ�����������ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ������ϣ������õ����ӣ�������ԭ��Ӧ��п�������ã�п�Ǹ�����������������Һ�е�ͭ���ӵõ����Ӷ�����ͭ��
�����Ѷȣ�һ��
2��ѡ���� ��ͼΪEFC���ŷ��ù����������(TiO2)���������ѵ�װ��ʾ��ͼ����ԭ�����ڽϵ͵�������λ�£�TiO2(����)�е�������������Σ��������ֻʣ�´��ѡ�����˵������ȷ����
A�������ĵ缫��ӦʽΪ��2Cl����Cl2��+2e��
B�������ĵ缫��ӦʽΪ��TiO2 + 4e����Ti + 2O2��
C��ͨ���O2����Cl�����������ƶ�
D��ʯī�缫�������������仯
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
3������� ����Ч�ļ���ȼ�ϵ�ز��ò�Ϊ�缫���ϣ����缫�Ϸֱ�ͨ��CH4��O2�������ΪKOH��Һ��ij�о�С�齫��������ȼ�ϵ�ش�������Ϊ��Դ�����б����Ȼ�����Һ���ʵ�飬��ͼ��ʾ��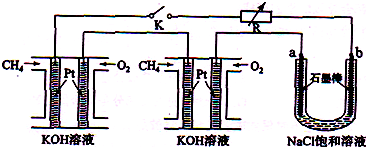
�ش��������⣺
��1������ȼ�ϵ�������������ĵ缫��Ӧ�ֱ�Ϊ?��?��
��2���պ�K���غ�a��b�缫�Ͼ����������������b�缫�ϵõ�����?������Ȼ�����Һ���ܷ�Ӧ����ʽΪ?��
��3����ÿ����ؼ���ͨ����Ϊ1L����״�������ҷ�Ӧ��ȫ����������ͨ�����صĵ���Ϊ?�������ڳ���F=9.65��l04C?mol-1��ʽ���㣩������ܲ������������Ϊ?L����״������
�ο��𰸣�
���������
�����Ѷȣ�һ��
4��ѡ���� ��ͼװ���У�AΪǦ���أ�C1��C2Ϊʯī�缫��B�ձ�����Ũ�Ⱦ�Ϊ0.1mol/L��H2SO3��KI�Ļ����Һ100mL������˵����ȷ����?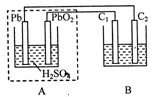
A��Ǧ���ع���һ��ʱ���A����Һ��PH��С
B����B�ձ���I-��Ũ�Ƚ�Ϊ0.05mol/Lʱ��A�����ĵ�
H2SO3�����ʵ���Ϊ0.025mol
C����C1��C2��������ʼ��������ʱ����������3.6��1022�����Ӵӵ�·������
D��Ǧ���ع���ʱ�������缫��ӦʽΪ��PbO2��2e -+ H2SO3 ��PbSO4+2H2O +SO42-
�ο��𰸣�B
�����������
�����Ѷȣ���
5��ѡ���� ���������ҺΪ��������ˮ��Һ������ȼ�ϵ�ص�ⱥ��̼������Һһ��ʱ�䣬������ʱ�¶Ȳ������ö��Ե缫������˵����ȷ����( ��)
A������ظ�������m g����ʱ����������ͬʱ��m g��������
B����صĸ�����ӦʽΪ��O2��2H2O��4e-=4OH-
C������c(Na2CO3)���䣬����Һ���о�������
D��ȼ�ϵ����c(KOH)���䣻��������ҺpH���
�ο��𰸣�C
���������A��������ӦΪ��H2��2e���T2H+����H2+2e��+2OH-�TH2O������������mg����ʱ��ת�Ƶĵ��ӵ����ʵ���Ϊmg ��2g/mol �� 2= mmol�����������ĵ���Ϊmmol��������ӦΪ��2H++2e���TH2���������������������Ϊm�� 2 mol��2g/mol=mg����A����
B����ص�������ӦʽΪ��O2��2H2O��4e-=4OH-����B����
C�����ݵ缫����ʽ��֪���Na2SO4ˮ��Һʵ���ǵ���ˮ������Na2SO4ˮ�ܵ�Ũ�Ȳ��䣬����Һ���о�����������C��ȷ��
D��ȼ�ϵ�ص��ܷ�ӦΪO2+2H2�T2H20��ԭ�����c��KOH����С��������ҺpH��С����D����
��ѡC��
���������⿼��ԭ��غ͵���֪ʶ������ע��缫����ʽ����д��Ϊ���ô�����Ŀ�Ĺؼ�֮����
�����Ѷȣ���