时间:2025-06-26 01:01:07
1、填空题 A、B、C、D、E为五种元素的单质,其余为化合物。其中只有E为金属元素,五种元素的原子序数按B、D、C、A、E顺序依次增大,D、C元素在周期表中位置相邻,在一定条件下,B分别和A、C、D化合生成甲、乙、丙,乙、丙每个分子中均含有10个电子;C和D化合可得丁。各物质相互转化关系如下图: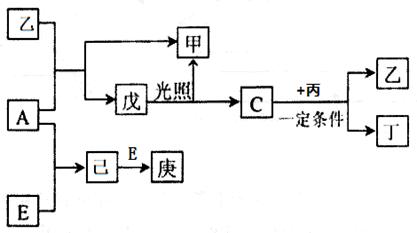
请回答下列问题:
(1)写出E元素在周期表的位置?。
(2)戊的名称为_________________;用途?(只写一种)。
(3)写出实验室制取A反应的离子方程式_________________________________。
(4)常温下A与足量的丙发生反应生成单质D,写出该反应的化学方程式
____________________________________________________________________。
(5)写出足量E和稀硝酸反应的化学方程式:
_______________________________________________________________________。
(6)实验室配制庚溶液的方法是______________________________________________。
参考答案:(1)第四周期第Ⅷ族 (2分)
(2)次氯酸?(1分)做漂白剂 (其他合理均给分)(1分)
(3)MnO2 + 4H+ + 2Cl― Mn2+ + Cl2↑ + 2H2O (2分)
Mn2+ + Cl2↑ + 2H2O (2分)
(4)3Cl2+8NH3=N2+6NH4Cl? (3分)
(5)3Fe +8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O? (3分)
(6)向盐酸中加入适量的FeCl2晶体,(1分)然后加水稀释,并加入少许铁粉。(1分)
本题解析:已知B分别和A、C、D化合生成甲、乙、丙,乙、丙每个分子中均含有10个电子,又知B原子序数最小,推测B为H元素,戊光照分解得到甲和C,则戊是HClO。
(1)E为Fe,位于第四周期第Ⅷ族
(2)戊为HClO,可做漂白剂。
(3)实验室制备氯气,注意离子方程式的书写。
(4)氯气可以氧化氨气,得到氮气。
(5)铁和稀硝酸反应,得到一氧化氮。
(6)制备FeCl2溶液,需要考虑防止亚铁离子的水解和防氧化。
本题难度:一般
2、推断题 根据下列框图关系填空,已知反应①、③是工业生产中的重要反应,D、E常温下为气体、X常温下为无色液体,H与E相对分子质量之间的关系为:Mr(H)-Mr(E)=34,又知C焰色反应通过蓝色钴玻璃火焰呈紫色。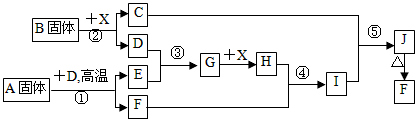
(1)固体B的电子式为_______________,其中所包含的化学键有_______________。
(2)固体A的化学式为_______________,其中非金属元素的化合价为_______________。
(3)反应④的离子方程式_________________________。反应⑤的化学方程式_____________________。
(4)用铜作电极电解H溶液,阳极的电极反应式是_________________________。
(5)若生成16gE,放出106.5kJ热量,则1mol A与足量D反应放出热量为:____________kJ。
参考答案:(1) ;离子键、共价键(或非极性键)
;离子键、共价键(或非极性键)
(2)FeS2;-1
(3)Fe2O3+6H+==2Fe3++3H2O;Fe2(SO4)3+6KOH=2Fe(OH)3↓+3K2SO4
(4)Cu-2e=Cu2+
(5)852
本题解析:
本题难度:困难
3、填空题 (每空2分,共12分)已知金属氧化物A和金属单质B在高温条件下反应生成C和D的同时放出大量的热;将F的饱和溶液滴入沸水中,煮沸可得到以H为分散质的红褐色液体。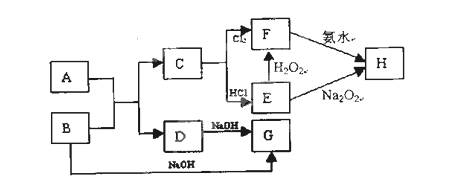
(1)红褐色液体中H粒子的直径大小范围?。
(2)写出D、E的化学式:D?、E?
(3)写出E的酸性溶液与双氧水反应的离子方程式?。
(4)写出F溶液中阳离子的检验方法:??离子方程式为?。
参考答案:(每空2分,其1 2分)
(1)? 1—100nm。
(2)D:Al2O3、E:? FeCl2
(3)? 2Fe2++H2O2+2H+=2Fe3++2H2O?。
(4)取少量F溶液与试管中,滴加几滴KSCN溶液,若变红,说明有Fe3+存在,否则没有。
Fe3++3SCN-=Fe(SCN)3。
本题解析:由图知H为氢氧化铁胶体,C为铁,D为Al2O3,A为Al,B为Fe2O3,E为FeCl2,F为FeCl3,G为NaAlO2.则⑶反应为2Fe2++H2O2+2H+=2Fe3++2H2O。Fe3+的检验可用KSCN溶液。
本题难度:一般
4、选择题 X、Y、Z是中学化学中三种常见元素的单质,甲、乙是两种常见的化合物,相互间有如图转化关系(未注明反应条件),下列说法不正确的是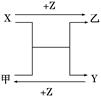
A.若X为金属单质,Y为非金属固体单质,则Z为O2
B.若X、Y均为金属单质,则甲不可能为黑色固体
C.若X为金属单质,Y为非金属气体单质,则乙可能为黑色固体
D.若X、Y均为非金属固体单质,则Z可能为O2
参考答案:B
本题解析:A、X为镁,Y为碳,Z为氧气,正确;B、若X为铝,Y为铁,Z为氧气,甲可以为四氧化三铁黑色物质,错误;C、X为铁,Y为氢气,Z为氧气,甲为水,乙为四氧化三铁,正确;D、X为碳,Y为硅,Z为氧气,甲为二氧化硅,乙为一氧化碳。
本题难度:一般
5、推断题 已知A、B、C是中学化学中的常见物质,它们在一定条件下有如下转化关系 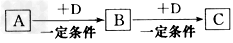
(1)若A能使湿润的红色石蕊试纸变蓝;C为红棕色气体。则A转化为B的化学反应方程式为________________________
(2)若D是具有氧化性的单质,A元素属于短周期主族金属元素,则C的化学式为________
(3)若D是金属,C溶液在贮存时应加入少量D,其理由是_____________________ (用必要的文字和离子方程式说明)。
(4)若D是一种常见的温室气体;A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子。则B转化为C的离子方程式为_____________________。
(5)若D为氯碱工业的主要产品,B具有两性,则C溶液中除氢氧根离子外还存在的阴离子为_________(填化学式)。
(6)若A、B、C均为氧化物,D是一种黑色固体非金属单质,则B分子的结构式为______________。
(7)若A的体积分数为75%的溶液可用作医疗消毒剂;B与新制氢氧化铜共热,有砖红色沉淀生成。则A生成B的化学方程式是__________________。
参考答案:(1)4NH3+5O2 4NO+6H2O
4NO+6H2O
(2)Na2O2
(3)加入少量铁,防止Fe2+被氧化为Fe3+,即2Fe3++Fe=3Fe2+
(4)CO2+CO32-+H2O=2HCO3-
(5)AlO2-{或[Al(OH)4]-)
(6)O=C=O
(7)2CH3CH2OH+O2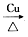 2CH3CHO+2H2O
2CH3CHO+2H2O
本题解析:
本题难度:一般