时间:2025-06-26 00:42:19
1、选择题 下列叙述正确的是
A.c(NH)相等的(NH4)2SO4溶液、(NH4)2Fe(SO4)2溶液和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2]<c[(NH4)2SO4]<c(NH4Cl)
B.0.1 mol・L-1的CH3COOH溶液加水稀释,溶液中c(OH-)减小
C.0.2 mol・L-1 HCl溶液与等体积0.05 mol・L-1 Ba(OH)2溶液混合后,溶液的pH=1
D.0.2 mol・L-1的NaHCO3溶液中c(H+)+c(H2CO3)=2c(CO)+c(OH-)
2、选择题 用0.10mol/L的NaOH溶液滴定100.0mL0.10mol/LHCl溶液时,滴定误差在±0.1%以内,反应完毕后溶液的pH变化范围是
A.6.9~7.1
B.4.3~9.7
C.3.6~10.4
D.以上都不正确
3、填空题 (15分)甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455 kJ/mol,甲醚可作燃料电池的燃料。
(1)写出甲醚燃烧的热化学方程式 ;已知H2(g)和C(s)的燃烧热分别是285.8 kJ・mol-1、393.5 kJ・mol-1;计算反应4C(s)+6H2(g)+O2(g)==2CH3OCH3 (g)的反应热为 ;
(2)工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+2CO2(g) CH3OCH3(g)+3H2O(g) △H<0
CH3OCH3(g)+3H2O(g) △H<0
①一定温度下,在一个固定体积的密闭容器中进行该反应.下列能判断反应达到化学平衡状态的是
______(选填编号,注意大小写)
a.c(H2)与c(H2O)的比值保持不变
b.单位时间内有2mol H2消耗时有1mol H2O生成
c.容器中气体密度不再改变
d.容器中气体压强不再改变
②温度升高,该化学平衡移动后到达新的平衡,CH3OCH3的产率将
________(填“变大”、“变小”或“不变”,下同),混合气体的平均式量将__________;
(3)以甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池的负极反应式为____________________;
(4)用(3)中的燃料电池为电源,以石墨为电极电解500 mL滴有酚酞的NaCl溶液,装置如图所示: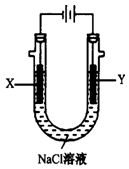
请写出电解过程中Y电极附近观察到的现象 ;当燃料电池消耗2.8 LO2(标准状况下)时,计算此时:NaCl溶液的pH= (假设溶液的体积不变,气体全部从溶液中逸出)。
4、选择题 现有常温下的四种溶液(如下表),下列有关叙述中正确的是(?)
| ? | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
5、选择题 下列叙述正确的是
A.把纯水加热,水的电离程度增大,但水仍然是中性的,pH=7
B.在醋酸溶液中加入少量的CH3COONa(s),测得pH变大,主要原因是CH3COONa水解呈碱性,中和醋酸电离的H+
C.pH=3的醋酸溶液,稀释至10倍后pH<4
D.相同浓度的CH3COONa溶液与Na2CO3溶液相比,Na2CO3溶液的pH小