时间:2025-06-26 00:27:37
1、填空题 下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。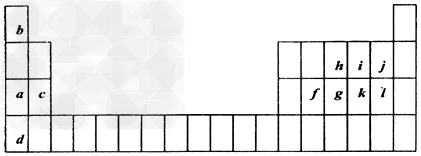
请你根据表中所给元素,回答下列问题:
(1)在短周期的所有元素中________的原子半径与_________?的原子半径之比最小(不包括稀有气体)(填元素符号)。
(2)金属性最强的元素与氧气反应生成化合物的化学式是__________(填两种即可),j和k氢化物比较,稳定性强的是?__________(填写氢化物化学式)。
(3)海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂,其单质做消毒杀菌剂的原因是____________(用化学方程式表示)
(4)常温下某液态化合物只含上述元素中的两种,分子中原子个数比1:1,请你仅用一个化学方程式表示该液态化合物既有氧化性又有还原性__________________。
2、推断题 短周期元素A、B、C、D中,0.5mol?A元素的离子得到6.02×1023个电子被还原为中性原子,0.4g?A的氧化物恰好与100ml?0.2mol/L的盐酸完全反应,A原子核内质子数目与中子数目相等,B元素原子核外第三层电子数目比第一层多1个,C-比A元素的离子多1个电子层,D元素的原子核外第二层比第一层多2个电子。回答下列问题:
(1)A、B、C、D四种元素的名称分别是_______、_______、_______、_______;
(2)C-的结构示意图为_______;D元素在周期表中的位置是__________;
(3)元素D的最简单气态氢化物的电子式为____,其分子的结构特点是具有_____结构,在一定条件下该氢化物可与单质C发生取代反应,若将等物质的量的该氢化物与单质C混合,在一定条件下充分反应后,生成物中物质的量最大的是_______(用化学式填写);
(4)工业上冶炼单质A的化学方程式为_____________________________________;
(5)工业上常用单质B冶炼难熔的金属,写出氧化铁和单质B在高温下反应的化学方程式_________________,该反应属于______反应(填“放热”或“吸热”);
(6)写出工业上用石英晶体与D的一种单质生产半导体材料的化学反应方程式_________________________;
(7)将D的单质在足量的氧气中完全燃烧,所得产物的结构式为____________。
3、选择题 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。下列说法正确的是 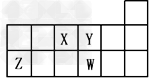
[? ]
A.元素Z位于元素周期表中第3周期第ⅠA族
B.原子半径的大小顺序为:rW>?rZ?>rY>?rX
C.Y、W元素的氢化物,其化学式都为H2R
D.离子Y2-和Z3+的核外电子数和电子层数都相同
4、选择题 下列化合物中阴阳离子半径之和最大的离子化合物是
A.NaF
B.NaCl
C.SO2
D.CaCl2
5、简答题 ①②③④⑤⑥六种元素,在元素周期表中的位置如图所示.回答下列问题:
| ⅠA | 0 ① ⅡA | … ⅢA ⅣA ⅤA ⅥA ⅦA ② ③ ④ ⑤ ⑥ |