时间:2025-06-26 00:20:09
1、选择题 在一定温度下,可逆反应A(气)+3B(气)  2C(气)达到平衡的标志是(? )?
2C(气)达到平衡的标志是(? )?
A.A、B、C的分子数比为132?
B.A、B、C的浓度相等
C.C生成的速率与C分解的速率相等?
D.单位时间生成n mol A,同时生成3n mol B
2、选择题 在一定条件下,已达平衡的可逆反应:2A(g)+B(g)  ?2C(g),下列说法中正确的是?(?)
?2C(g),下列说法中正确的是?(?)
A.平衡时,此反应的平衡常数K与各物质的浓度有如下关系:K=
B.改变条件后,该反应的平衡常数K一定不变
C.如果改变压强并加入催化剂,平衡常数会随之变化
D.若平衡时增加A和B的浓度,则平衡常数会减小
3、填空题 (12分)在100 ℃时,将0.40 mol二氧化氮气体充入2 L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
4、选择题 可逆反应H2(g) + I2(g) 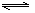 2HI(g)达到平衡的标志是
2HI(g)达到平衡的标志是
A.H2、I2、HI的浓度相等
B.H2、I2、HI的浓度之比为1:1:2
C.混合气体的平均相对分子质量不变
D.混合气体的颜色不再改变
5、选择题 对于可逆反应2NO2 N2O4,下列说法能证明反应已达平衡状态的是?
N2O4,下列说法能证明反应已达平衡状态的是?
⑴温度和体积一定时,某一生成物浓度不再变化;
⑵温度和体积一定时,容器内压强不再变化;
⑶条件一定,混合气体的平均相对分子质量不再变化;
⑷温度和体积一定时,混合气体的颜色不再发生变化;
⑸温度和压强一定时,混合气体的密度不再发生变化;