时间:2025-06-26 00:19:26
1、填空题 (1)现有下列基本粒子:1H、2H、3H、40K、40Ca、请回答下列问题:
其中,它们分属______种元素,属于氢元素的核素有______种,互为同位素的原子为______.质量数相等的粒子为______
(2)许多元素有多种核素,而且在自然界中各种核素都有固定的原子分数.如氧元素存在16O、17O、18O三种核素,氢元素有1H、2H、3H三种核素,请你估计,16O、17O、1H、2H三种核素最多可能组成______种水分子,现有20.0g由2H和16O组成的水分子,其中含质子的物质的量为______,中子的个数为______
(3)微粒AXn-核外有18个电子,则它的核电荷数为______.
参考答案:(1)1H、2H、3H、40K、40Ca分别属于H,K,Ca三种元素,氢元素的核素有3种1H、2H、3H,1H、2H、3H互为同位素,质量数相等的粒子为40K、40Ca,
故答案为:3;3;1H、2H、3H;40K、40Ca;
(2)因1个水分子是由两个氢原子和1个氧原子构成,则16O与2个1H、16O与2个2H、17O与2个1H、17O与2个2H、16O与1H和2H、17O与1H和2H共组成6种水分子;由2H和16O组成的水分子中,相对分子质量为2×2+16=20,2H含有1个质子,1个中子,16O含有8个质子,8个中子,
20克由2H和16O组成的水的物质的量为:20g20g/mol=1mol,
含质子数为:1×(2×1+8)=10mol,中子数为:1×(2×1+8)=10mol,即10NA个,故答案为:6;10mol;10NA;
(3)阴离子的核电荷数=核内质子数=核外电子数-电荷数=18-n,故答案为:18-n.
本题解析:
本题难度:一般
2、选择题 A元素的最高正化合价和负化合价的绝对值之差6,B元素与A元素的原子次外层上的电子数均为8,A与B可形成化合物BA2,则该化合物是?
[? ]
A.MgCl2
B.CaF2
C.SiO2
D.CS2
参考答案:A
本题解析:
本题难度:简单
3、选择题 X、Y、Z三种短周期元素,原子半径的大小关系为r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质在在适当条件下可发生如下变化,其中B和C均为10电子分子。下列说法中不正确的是? 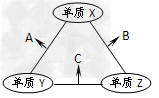
[? ]
A.X元素位于ⅥA?
B.B的沸点大于C的沸点
C.A能溶解于B中?
D.A和C不可能发生氧化还原反应
参考答案:CD
本题解析:
本题难度:一般
4、选择题 下列物质性质递变正确的是( )
A.原子半径:C、Al、K依次增大
B.热稳定性:HF、NH3、SiH4依次增强
C.水化物的酸碱性:NaOH、Al(OH)3、Mg(OH)2碱性减弱
D.非金属性:Cl、P、S依次增强
参考答案:A.C核外有2个电子层,电子层数最小,则半径最小,K原子核外有4个电子层,电子层数最多,半径最大,则有原子半径:C、Al、K依次增大,故A正确;
B.非金属性:F>N>Si,元素的非金属性越强,对应的氢化物越稳定,则有:热稳定性:HF、NH3、SiH4依次减弱,故B错误;
C.金属性:Na>Mg>Si,元素的金属性越强,对应最高价氧化物的水化合物的碱性越强,则有NaOH、Mg(OH)2、Al(OH)3碱性减弱,故C错误;
D.同周期元素从左到右元素的非金属性逐渐增强,则非金属性:Cl、P、S依次减弱,故D错误.
故选A.
本题解析:
本题难度:简单
5、选择题 下列各组物质不能实现直接转化的是?
A.S→SO2→H2SO4→MgSO4
B.Cu→CuCl2→Cu(NO3)2→Cu(OH)2
C.Al→Al2O3→Al(OH)3→NaAlO2
D.Na→Na2O→Na2CO3→NaCl
参考答案:C
本题解析:因为Al2O3不与水反应,Al2O3→Al(OH)3不能直接转化,故C项错误。
本题难度:一般