时间:2025-06-26 00:18:36
1、选择题 下列关于充电电池的叙述,不正确的是( )。
A.充电电池的化学反应原理是氧化还原反应
B.充电电池可以无限制的充电放电
C.充电是使放电时的氧化还原反应逆向进行
D.较长时间不使用电池时,最好将电池取出并妥善存放
参考答案:B
本题解析:充电电池理论上是可以永久重复利用的,但在实际应用中总会因为性能等原因而使电解质溶液或者电极变质而失效。所以实际情况下充电电池是不能无限制重复使用的。
本题难度:一般
2、填空题 2009年12月7日~18日在丹麦首都哥本哈根召开了世界气候大会,商讨《京都议定书》一期承诺到期后的后续方案,即2012年至2020年的全球减排协议,大会倡导“节能减排” 和“低碳经济”,降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。过渡排放CO2会造成“温室效应”,科学家正在研究如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应: CO2(g)+3H2(g)
CO2(g)+3H2(g) CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ·mol-1)的变化:
CH3OH(g)+H2O(g),下图表示该反应过程中能量(单位为kJ·mol-1)的变化: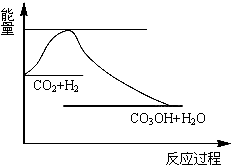
(1)关于该反应的下列说法中,正确的是____________(填字母)。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),经测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),经测得CO2和CH3OH(g)的浓度随时间变化如图所示。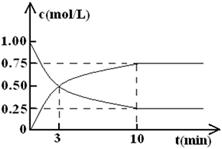
①从反应开始到平衡,CO2的平均反应速率v(CO2)= 。
②该反应的平衡常数表达式K= 。
③下列措施中能使化学平衡向正反应方向移动的是 (填字母)。
A.升高温度
B.将CH3OH(g)及时液化抽出
C.选择高效催化剂
D.再充入l molCO2和3 molH2
(3)25℃,1.01×105Pa时,16g液态甲醇完全燃烧,当恢复到原状态时,放出369.2kJ的热量,写出该反应的热化学方程式:___________________________________________。
(4)选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此电池的负极应加入或通入的物质有__________ _____;其正极的电极反应式是:_____________________________________。
参考答案:(1) C(2分)
(2) ① 0.075 mol·L-1·min-1(2分,单位错漏扣1分)
② 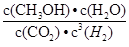 (2分)
(2分)
③ BD(2分,只有填写BD才可得分,其他填法均不能得分)
(3)CH3OH(l)+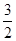 O2 =CO2(g)+2H2O(l) △H=-725.8 kJ·mol-1(3分,单位错漏扣1分)
O2 =CO2(g)+2H2O(l) △H=-725.8 kJ·mol-1(3分,单位错漏扣1分)
(4)甲醇、氢氧化钠、水(漏写一个扣1分,漏写两个或错写均不得分);O2+2H2O+4e-=4OH?(各2分)
本题解析:化学高考试题中的信息题常常和时事联系很紧密。
图像类试题一直在高考试题中保留,并且今后还会继续保留。这类题型能够考查学生对图形图像的抽象、概括和分析能力,对图像数据的处理能力。另处,预计今年电化学、化学平衡常数、反应热和熵变的判断将成为某些地区考题的热点,特别是第一届新课标高考的省区,故笔者在设计试题时安排了上述的内容。
本题集化学反应速率与化学平衡、反应热和电化学知识为一体,通过甲醇联系起来,可谓“一题多点”,这样设计有利于考查学生综合运用所学知识解决实际问题的能力。笔者对近年来的各省区高考试题分析,这样的题型很有可能是今后高考命题的一个方向。本题难度适中,符合2010年高考考试大纲要求。
(1)通过图像可以看出,该反应是一个放热反应,因而△H<0;又由化学方程式CO2(g)+3H2(g) CH3OH(g)+H2O(g)得,反应后气体分子的物质的量减小,故△S<0,所以C项正确;
CH3OH(g)+H2O(g)得,反应后气体分子的物质的量减小,故△S<0,所以C项正确;
(2)①因容器的体积为l L,CO2的起始浓度为1.00 mol/L,平衡浓度为0.25 mol/L,反应时间为10 min,所以CO2的平均反应速率v(CO2)= 0.075 mol·L-1·min-1;
①该反应的平衡常数表达式K= 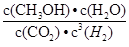 ;
;
③由于该反应的正反应是放热反应,所以升高温度,平衡会逆向移动,A项错误;将CH3OH(g)及时液化抽出,相当于减小生成物的浓度,使平衡正向移动,B项正确;催化剂只能影响反应速率,不能使平衡发生移动,C项错误;再充入l molCO2和3 molH2相当于增大体系的压强,化学平衡向气体体积缩小的方向(即正向)移动,故D项正确。
(3)根据题意, 16g 液态甲醇,即0.5 mol CH3OH完全燃烧,当恢复到原状态时,放出369.2kJ的热量,可以计算出1 mol CH3OH完全燃烧应放出热量725.8 kJ,故该反应的热化学方程式:CH3OH(l)+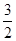 O2(g)=CO2(g)+2H2O(l) △H=-725.8 kJ·mol-1;
O2(g)=CO2(g)+2H2O(l) △H=-725.8 kJ·mol-1;
(4)作为电池的负极应是失去电子的物质,发生的是氧化反应;正极处发生的是还原反应。原料为氢氧化钠、甲醇、水和氧气,显然氧化的氧化性强,是得到电子的物质,甲醇是失去电子的物质,而氢氧化钠、水是电解质溶液。所以在电池的负极应加入或通入的物质有甲醇、氢氧化钠和水。正极为氧气得电子,发生的电极反应式为O2+2H2O+4e-=4OH?。
本题难度:困难
3、填空题 (7分)
熔融碳酸盐燃料电池(MCFS),发明于1889年。现有一个碳酸盐燃料电池,以一 定比例Li2CO3和Na2CO3熔融混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为1:1)直接作燃料,其工作原理如图所示。
定比例Li2CO3和Na2CO3熔融混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为1:1)直接作燃料,其工作原理如图所示。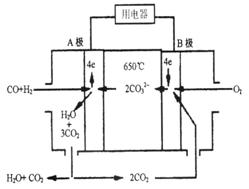
请回答下列问题:
(1)B极发生____(填“氧化”或“还原”)反应
(2)电池总反应为___________________________________________。
(3)以 此电源电
此电源电 解足量的CuSO4溶液,阳极产生气体0.56 L(已换算为标况),则阴极产物的质量为 g。电解后溶
解足量的CuSO4溶液,阳极产生气体0.56 L(已换算为标况),则阴极产物的质量为 g。电解后溶 液体积为1 L,溶液的pH约为 。
液体积为1 L,溶液的pH约为 。
(4)电池中的电解质碳酸钠形成的水溶液体系不能用带玻璃塞的试剂瓶保存,其原因是
(用化学方程式表示)
参考答案: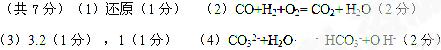
本题解析:略
本题难度:一般
4、选择题 下图是氢氧燃料电池构造示意图。关于该电池说法中错误的是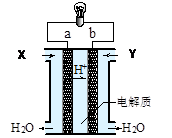
A.a极是负极
B.正极的电极反应是:O2+2H2O+4e- = 4OH-
C.电子由a通过灯泡流向b
D.通入的气体Y为O2
参考答案:B
本题解析:A项:从图中可以看到,H+移向b极,可知b极为负极,a极为正极,故错。C项:电子是由b通过灯泡流向a的,故错。D项:b极为负极,通入的是H2,故错。故选B。
点评:本题考查的是燃料电池的知识,解答本题先从H+的移向入手,在原电池中阳离子移向负极,即可作答本题。
本题难度:简单
5、选择题 最新研制的一种由甲醇和氧气以及强碱作电解质溶液的新型手机电池。下列有关此电池的叙述错误的是
[? ]
A.正极电极反应:O2+2H2O+4e-=4OH-
B.负极电极反应:CH3OH+8OH--6e-=CO32-+6H2O
C.电池在使用过程中电解质溶液的pH升高
D.当外电路通过0.6mol电子时,理论上消耗甲醇3.2g
参考答案:C
本题解析:
本题难度:一般