时间:2025-06-26 00:07:10
1、选择题 用下图表示的一些物质或概念间的从属关系中不正确的是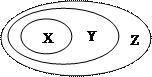
| | X | Y | Z |
| A. | 酸 | 化合物 | 纯净物 |
| B. | 电解质 | 盐 | 化合物 |
| C. | 胶体 | 分散系 | 物质 |
| D. | 碱性氧化物 | 氧化物 | 化 合物 合物 |
2、选择题 下列物质是非电解质的是 ( )
A.NH3
B.(NH4)2SO4
C.Cl2
D.CH3COOH
3、填空题 (6分)在下列物质中选择溶于水后可以电离的物质,并写出相应的电离方程式(有几个写几个):①硝酸铵(NH4NO3) ②葡萄糖[C6H12O6] ③氢氧化钡[Ba(OH)2] ④硫酸(H2SO4) ⑤四氯化碳(CCl4)
。
4、选择题 下列说法不正确的是
A.冰醋酸、消石灰、明矾、生石灰分别属于酸、碱、盐、氧化物
B.电解质在水溶液和熔融状态下均一定能导电
C.电解、电泳、电镀需要通电才可进行,而电离、原电池导致的腐蚀不需要通电
D.物质溶于水的过程中,一般有放热或吸热现象,因此溶解的操作不能在量筒中进行
5、填空题 ①现有下列物质:①盐酸 ② 纯碱③豆浆④烧碱⑤干冰⑥食盐水⑦氢气⑧泥水。
请根据它们所属的类别选择相应的序号填入下表中。
| 类别 | 单质 | 酸 | 碱 | 盐 | 氧化物 | 胶体 |
| 物质 | | | | | | |