时间:2025-06-26 00:07:10
1、选择题 下列电离方程式错误的是
A.NaHSO4 ="==" Na+ + H+ + SO42-
B.NaHCO3 ="==" Na+ + H+ +CO32-
C.MgCl2 ="==" Mg2+ + 2Cl-
D.Ba(OH)2 ="==" Ba2+ + 2OH-
2、填空题 (1)(4分)以下四组物质中都有一种与其他物质在分类上不同,试分析每组物质的组成或特点,将这种物质找出来。
A.CaO、Na2O、CO2、CuO
B. H2、Cl2、P、Cu
C.氢氧化镁、烧碱、纯碱、熟石灰
D.洁净的空气、用排空气法收集的SO2、盐酸、冰水混合
A ;B ;C ;D 。
(2)(3分)下列各组中两瓶无标签的无色溶液,不用其他试剂就能鉴别出来的是 ;(填序号)
(1)NaOH和AL2(SO4)3 (2)HCl和KAlO2 (3)Na2CO3和HCl
(4)NaHCO3和NaOH (5)Ca(HCO3)2和NaOH
(3)(3分)溶解 Al2O3 、Fe2O3 的混合物用去 100 mL 0.1 mol/L 的盐酸。如果将所得溶液加入 NaOH 欲产生最大量沉淀,需用 1 mol/L 的NaOH溶液 毫升?
3、选择题 下列各组物质,按混合物、单质、化合物顺序排列正确的是
A.空气、臭氧、胆矾
B.碘酒、白磷、盐酸
C.干冰、氮气、冰
D.生石灰、液氧、大理石
4、选择题 下列物质中,不属于电解质的是( )
A.NaCl
B.H2SO4
C.KOH
D.盐酸
5、填空题 根据要求回答下列各题
(Ⅰ)现有 ①铝 ②NH3③氢氧化钠溶液 ④液态氯化氢 ⑤AgCl固体⑥冰醋酸 ⑦蔗糖,填空回答(填序号):
以上物质中(1)属于电解质的是 ;(2)属于非电解质的是 ;
(3)属于强电解质的是 ;(4)能导电的是 。
(Ⅱ)写出下列反应的化学方程式:
①有NaHCO3生成的化合反应
② 有MgCl2参加的分解反应
③ 有Fe2O3参加的置换反应
④ 有HNO3生成的复分解反应
(Ⅲ).同温同压条件下,同体积的CH4和SO2的质量之比是 ;同质量的CH4和SO2的体积之比是 ;若两者所含原子个数总数相等,则CH4和SO2的质量之比是 。
(Ⅳ)把铁片和石墨棒用下列a、b两种方式放在盛有稀硫酸钠溶液和酚酞试液混合溶液的玻璃器皿中,经过一段时间后,首先观察到溶液变红的区域是 (填序号)。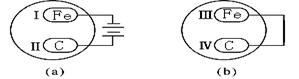
A.Ⅰ和Ⅲ附近
B.Ⅰ和Ⅳ附近
C.Ⅱ和Ⅲ附近
D.Ⅱ和Ⅳ附近