ʱ��:2025-06-25 23:45:55
1��ѡ���� �����й�ԭ�ӽṹ��Ԫ�������ɱ�����ȷ����
[? ]
��ԭ������Ϊ15��Ԫ�ص�����ϼ�Ϊ��3
�ڢ�A��Ԫ����ͬ�����зǽ�������ǿ��Ԫ��
�۵ڶ����ڢ�A��Ԫ�ص�ԭ�Ӻ˵������������һ��Ϊ6
��ԭ������Ϊ12��Ԫ��λ��Ԫ�����ڱ��ĵ������ڢ�A��
A���٢�
B���٢�
C���ڢ�
D���ۢ�
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2��ѡ���� �±��������У�A��B��C��D��E������ͬһ�ֶ�����Ԫ�أ�����A�ǵ��ʣ�B����������̬�⻯�C��D�������E��D��ˮ��Ӧ�IJ���������֮��ͨ��һ����Ӧ����ʵ�ֱ�����ʾת������(����)
| ���ʱ�� | ����ת����ϵ | A | D | E |
| �� | 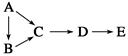 | Si | SiO2 | H2SiO3 |
| �� | S | SO3 | H2SO4 | |
| �� | Na | Na2O2 | NaOH | |
| �� | N2 | NO2 | HNO3 |
�ο��𰸣�B
�����������Si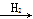 SiH4��Si��O2ֱ������SiO2��Siֻ������һ����������SiO2������H2O��Ӧ����H2SiO3����S
SiH4��Si��O2ֱ������SiO2��Siֻ������һ����������SiO2������H2O��Ӧ����H2SiO3����S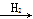 H2S��S
H2S��S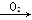 SO2��H2S
SO2��H2S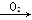 SO2��SO2
SO2��SO2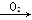 SO3
SO3 H2SO4����ȷ����Naû����̬�⻯���N2
H2SO4����ȷ����Naû����̬�⻯���N2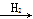 NH3��N2
NH3��N2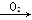 NO��NH3
NO��NH3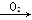 NO��NO
NO��NO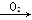 NO2
NO2 HNO3��
HNO3��
�����Ѷȣ�һ��
3������� ����ѡһ�������ʽṹ�����ʡ�
��֪A��B��C��D��E����Ԫ�ض���Ԫ�����ڱ���ǰ20��Ԫ�أ�ԭ��������������E�����������Ų�ʽΪ4s2��A��B��C��D����Ԫ����Ԫ�����ڱ��е����λ�����±���ʾ��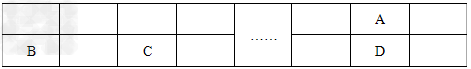
����������Ϣ���ش��������⣺
��1��Ԫ��C��Ԫ�����ڱ��е�λ����__________��D�ĵ����Ų�ʽΪ��____________��
��2��A��D���⻯���У��е�ϸߵ���_______��ԭ����__________________��A��B�������У��뾶��С����__________�������ӷ��ţ���
��3��A��E��������ӻ�����侧��(�������ھ����о��д����Ե���С�ظ���Ԫ)�ṹ��ͼ��ʾ���������á���ʾ��λ�ڸ�������Ķ�������ģ��������á�������ʾ����λ��С���������ģ����û�����ĵ���ʽ��_______________�� 
��4��A��E������ľ���1/8�����Ϊ2.0��10-23cm3����A��E��ɵ����ӻ�������ܶȣ�����ʽ�����㣨�������һλС������_______________________________��
�ο��𰸣���1����������A��1s22s22p63s23p5?
��2��A��A���⻯����Ӽ�����γ��������D���⻯�ﲻ�ܣ�Na��
��3�� ?
?
��4��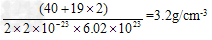
���������
�����Ѷȣ�һ��
4������� �ö�����Ԫ�ص�Ԫ�ط��Żش������й����⣺
��1�������к�����Ԫ����______��
��2�����ԭ��������С��Ԫ����______��
��3���ؿ��к�������λ�Ľ���Ԫ����______��
��4������������ˮ��������Ե�Ԫ����______��
�ο��𰸣���1����������Ҫ�ɷ�Ϊ�������������������������ԼΪ78%��������к�����Ԫ��ΪNԪ�أ��ʴ�Ϊ��N��
��2��H�����ԭ������Ϊ1�������ԭ��������С��Ԫ����HԪ�أ��ʴ�Ϊ��H��
��3���ؿ���Ԫ�صĺ����϶��ΪO��Si��Al��Ca���������Ľ���Ԫ��ΪAl���ʴ�Ϊ��Al��
��4�������������������ԣ�����������ˮ��������Ե�Ԫ����Al���ʴ�Ϊ��Al��
���������
�����Ѷȣ���
5��ѡ���� ���������еķǽ���Ԫ�أ����⻯�����ȶ����ǣ�������
A�����ɿ������ʯ����ҪԪ��
B�������к�������Ԫ��
C�������ڳ�������Һ̬��Ԫ��
D���ؿ��к�������Ԫ��
�ο��𰸣�A�����ɿ������ʯ����ҪԪ��ΪSiԪ�أ�
B�������к�������Ԫ��ΪNԪ�أ�
C�������ڳ�������Һ̬��Ԫ��ΪBrԪ�أ�
D���ؿ��к�������Ԫ��ΪOԪ�أ�
��ǽ�����O��N��Br��Si��
����OԪ�ص��⻯�����ȶ���
��ѡD��
���������
�����Ѷȣ���