ʱ��:2025-06-25 23:32:52
1��ʵ���� ����������������������ע����Һ���ش��������⡣
��1������װ��A��д��ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽ��?����ƿ�е�ʵ������Ϊ?��
��2����֤̼����ǽ����Ե����ǿ��(��֪���ԣ�H2SO3>H2CO3)����ѡ������A��B��C��D�������ӣ���B��C��D����ѡ����Լ��ֱ�Ϊ?��?��?����˵��̼�ķǽ����Աȹ�ǿ��ʵ��������?��
��3����֤SO2�������ԡ���ԭ�ԡ���ѡ��A��E��F����������A��E��F˳�����ӡ�
����֤��SO2�������Ե�ʵ��������?����Ӧ����ʽΪ��
?��
����֤��SO2���л�ԭ�ԣ���E�в�ȡ��ʵ�����Ϊ?����ʵ������Ϊ?����Ӧԭ��Ϊ?��
�ο��𰸣���1��Cu+2H2SO4(Ũ)  ?CuSO4+SO2��+2H2O��? 1��
?CuSO4+SO2��+2H2O��? 1��
ͭƬ��Һ�ɫ�������������ɣ���ƿ�п����а�ɫ�������� ?2��
��2��B��Na2CO3��Һ�� NaHCO3 ��Һ?C��KMnO4��Һ D��Na2SiO3��Һ ��
C��KMnO4��Һ����ɫ����Ʒ�첻��ɫ����D�г��ְ�ɫ������?��1�֣���4��
��3����H2S��Һ����dz��ɫ���dz���? 2H2S+SO2=3S��+2H2O?��1�ֹ�2��
��ͨ�������������ˮ��������������Һ������������Һ��������������һ�ֻ����������𰸾��ɣ����������а�ɫ�������ɡ�?��1�ֹ�2��
�����������Լ�д������ʽ Ba2++SO2+Cl2+2H2O=BaSO4��+4H++2Cl? ?2��
���������
��
 CuSO4+SO2��+2H2O����ƿ�е�ʵ������ΪͭƬ��Һ�ɫ�������������ɣ���ƿ�п����а�ɫ��������
CuSO4+SO2��+2H2O����ƿ�е�ʵ������ΪͭƬ��Һ�ɫ�������������ɣ���ƿ�п����а�ɫ�������������Ѷȣ�һ��
2��ʵ���� ��10�֣���ѧС��ͬѧ���ݻ�ѧ��ӦZn��2H2SO4(Ũ) ZnSO4��SO2����2H2O��ȡ22.4 L(��״��)SO2���塣ȡ65.0 gп����98%��ŨH2SO4(�ѣ�1.84 g��cm-3)110 mL��ַ�Ӧ��пȫ���ܽ⡣�����Ƶõ����壬��ͬѧ��Ϊ���ܻ���������Ϊ�ˣ���ѧС���ͬѧ���������ʵ��װ�ã�������ȡ���������̽����
ZnSO4��SO2����2H2O��ȡ22.4 L(��״��)SO2���塣ȡ65.0 gп����98%��ŨH2SO4(�ѣ�1.84 g��cm-3)110 mL��ַ�Ӧ��пȫ���ܽ⡣�����Ƶõ����壬��ͬѧ��Ϊ���ܻ���������Ϊ�ˣ���ѧС���ͬѧ���������ʵ��װ�ã�������ȡ���������̽����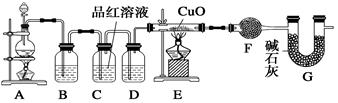
��ش��������⣺
��1��װ��A������Һ�����������Ϊ?��98%��ŨH2SO4(�ѣ�1.84 g/cm3)�����ʵ���Ũ����?��
��2����д�����������ķ�Ӧ�����ӷ���ʽ?��
��3����װ��B��Ϊ������SO2������ѡ�������Լ��е�?������ţ���
A��NaOH��Һ? B��ŨH2SO4? C��KMnO4��Һ?
�ڿ�֤ʵһ������п����һ������Ũ���ᷴӦ�����ɵ������л���������ʵ��������?��
�ο��𰸣���1����Һ©��? 18.4 mol/L?��2��Zn��2H+===Zn2+��H2��?
��3���� B�� ��װ��E�к�ɫ��ĩ���ɫ��F����ˮ����ͭ����ɫ?��ÿ��2�֣�
����������Ÿ����������Ƿ�Һ©����C��H2SO4��=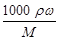 ��
��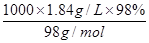 ��18.4?mol/L��?
��18.4?mol/L��?
��п��ϡ���ᷴӦ��������п�������������ӷ���ʽΪZn+2H+�TZn2++H2����
�Ǣٶ���������������������ܱ���Һ���գ����л�ԭ�ԣ��ܱ�ǿ��������Һ���գ�����������Һ�ʼ��ԣ����������Һ����ǿ�����ԣ�������������������Һ���������Һ���ն�������ѡB����?
���������л�ԭ�ԣ��ܽ���ɫ��CuO��ԭΪ��ɫ��Cu��������ˮ��ˮ��ʹ��ˮ����ͭ����ɫ������������������������ǣ�װ��E�к�ɫ��ĩ���ɫ��F����ˮ����ͭ����ɫ��
�����Ѷȣ�һ��
3��ѡ���� ����C��N��S�ǽ���Ԫ�ؼ��仯���������˵���У��������
A.���ʯ��ʯī��C60����̼Ԫ����ɵĵ��ʣ�����̼��ͬ��������
B.������������������γ��������Ҫ����
C.C��N��Sԭ�Ӱ뾶���������⻯���ȶ�������ǿ
D.���������£�̼�����ʶ�����Ũ���ᡢŨ���ᷢ����Ӧ
�ο��𰸣�C
���������
�𰸣�C
C ����ȷ��Ӧ�ǣ�ԭ�Ӱ뾶��S>C >N,�⻯���ȶ��ԣ�NH3 >CH4 >H2S
�����Ѷȣ���
4��ѡ���� �Ѻ���48%�����������Ƴ����ᣬ�����հ����Ƴ�����李�1 t���������������������Ƶ������()
A��1.06 t
B��1.98 t
C��2.14 t
D��2.26 t
�ο��𰸣�B
���������FeS2�е�S�ĺ���Ϊ ��100%=53.3%������Ŀ�����ṩ���������к���48%�����Բ�����FeS2���м��㣬����ݿ�ʯ�ĺ�������Sԭ���غ�ù�ϵʽ��
��100%=53.3%������Ŀ�����ṩ���������к���48%�����Բ�����FeS2���м��㣬����ݿ�ʯ�ĺ�������Sԭ���غ�ù�ϵʽ��
2S��2SO2��2SO3��2H2SO4��2(NH4)2SO4
64 t? 2��132 t
1 t��48%?m��(NH4)2SO4��
m����NH4)2SO4��="1.98" t
�����Ѷȣ���
5��ʵ���� [2012��������ʦ���С�����ʦ���С�����ʡʵ����ѧ�ڶ�������ģ��]��16�֣�ijͬѧΪ��̽��ͭ��Ũ����ķ�Ӧ������������ʵ�顣
��ʵ��1��ͭ��Ũ���ᷴӦ��ʵ��װ����ͼ��ʾ��
ʵ�鲽�裺
�������Ӻ�װ�ã����������ԣ������Լ���
�ڼ���A�Թ�ֱ��B��Ʒ����ɫ��Ϩ��ƾ��ƣ�
�۽�ͭ˿���������뿪Һ�档
��1��װ��A�з�����Ӧ�Ļ�ѧ����ʽΪ?��
��2��Ϩ��ƾ��ƺ���Ϊ�е���D�Ĵ��ڣ�B�е�Һ�岻�ᵹ������ԭ����?��
��3�����װ��ǰ������������Ϳ�ʹװ���в���������ȫ�����գ�Ӧ����ȡ�IJ���?��
��ʵ��2��ʵ���з����Թ��ڳ��˲�����ɫ�����⣬��ͭ˿���滹������ɫ����ף����п��ܺ�������ͭ����ͭ������ͭ���Լ����ڱε�������ͭ��
�������ϣ�
��������ͭ�����Ի����»ᷢ������������ԭ��Ӧ����Cu2+��ͭ���ʣ��������������գ�����ת��Ϊ����ͭ��
����ͭ������ͭ�����¶�������ϡ���ᣬ�������������գ���ͭ������ͭ��ת��Ϊ����ͭ�Ͷ�������
Ϊ���о��ijɷ֣���С��ͬѧ���ռ����㹻���Ĺ������������ͼ��ʵ�飺
��4�����м��������Ƿ�ϴ�Ӹɾ���ʵ�鷽����?��
��5�����������չ�����һ�������ķ�Ӧ�Ļ�ѧ����ʽΪ?��
��6�����ж��ڹ���ijɷֵ��ж��У���ȷ����(����ĸѡ��)?��
A��������У�CuS��Cu2S����ͬʱ����
B��������У�CuO��Cu2O������һ��
C�����������û��Cu2O����һ����Cu2S
D������������Cu2S
�ο��𰸣���16�֣���1��2H2SO4(Ũ)��Cu CuSO4��SO2����2H2O
CuSO4��SO2����2H2O
��2���Թ�A������ѹǿ��С��������D���ܽ����Թ�A��
��3����D�ܿ���A�д����������
��4��ȡ���һ��ϴ�Ӻ�����Һ�����Թ��У��μ���������Һ�����ް�ɫ������������˵������ϴ�Ӹɾ������а�ɫ�������ɣ���˵��δϴ�Ӹɾ�
��5��2CuS��3O2 2CuO��2SO2(����Ҳ��Ϊ�����ա�)
2CuO��2SO2(����Ҳ��Ϊ�����ա�)
��6��BCD
�����������6������Һ����ɫ��֪��������к�CuO��Cu2O������һ�֡�����CuS�ķ�Ӧ����ʽΪ2CuS��3O2 2CuO��2SO2���ɸ÷���ʽ�ɼ����2gCuS���պ������������0.33g������Cu2S�ķ�Ӧ����ʽΪCu2S��2O2
2CuO��2SO2���ɸ÷���ʽ�ɼ����2gCuS���պ������������0.33g������Cu2S�ķ�Ӧ����ʽΪCu2S��2O2 2CuO��SO2���÷�Ӧ�ǹ�����������ķ�Ӧ������Cuʱ�����������ӣ��������⣬�������һ������CuS��ͬʱCu2O��Cu2S����һ�֡����Ϸ���ֻ��A���ȷ��
2CuO��SO2���÷�Ӧ�ǹ�����������ķ�Ӧ������Cuʱ�����������ӣ��������⣬�������һ������CuS��ͬʱCu2O��Cu2S����һ�֡����Ϸ���ֻ��A���ȷ��
�����Ѷȣ�һ��