时间:2025-06-25 23:13:15
1、选择题 下列说法中正确的是
[? ]
A.汽油燃烧时将全部的化学能转化为热能
B.向饱和AgCl溶液中加入盐酸,Ksp变大
C.若存在简单阴离子R2-,则R一定属于第ⅥA族元素
D.最外层电子数较少的金属元素,一定比最外层电子数比它多的金属元素活泼
参考答案:C
本题解析:
本题难度:简单
2、选择题 向含有AgCl(s)的饱和AgCl溶液中加水,下列叙述正确的是
[? ]
A.AgCl的溶解度增大
B.AgCl的溶解度、Ksp均不变
C.Ksp(AgCl)增大
D.AgCl的溶解度、Ksp均增大
参考答案:B
本题解析:
本题难度:一般
3、选择题 已知常温下反应①NH3+H+ NH
NH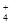 (平衡常数为K1),②Ag++Cl-
(平衡常数为K1),②Ag++Cl-
参考答案:
本题解析:
本题难度:一般
4、填空题 医学上在进行胃肠疾病的检查时,利用X射线对BaSO4穿透能力较差的特性,常用BaSO4做内服造影剂,这种检查手段称为钡餐透视。
(1)请写出BaSO4能作为钡餐透视的另外一个理由:________________________。
(2)请用文字叙述和离子方程式说明钡餐透视时为什么不用BaCO3?_________________________。
(3)某课外活动小组为探究BaSO4的溶解度,分别将足量BaSO4放入:
①5 mL水 ②20 mL 0.5 mol・L-1的Na2SO4溶液 ③40 mL 0.2mol・L-1的Ba(OH)2溶液 ④40 mL 0.1 mol・L-1的
H2SO4溶液中,溶解至饱和。
①以上各溶液中,c(Ba2+)的大小顺序正确的是__________,BaSO4的溶解度的大小顺序为_________(填序号)。
A.③>①>④>② B.③>①>②>④ C.①>④>③>② D.①>③>④>②
②已知25℃时,Ksp(BaSO4)=1.1×10-10,上述条件下,溶液③中的c(SO42-)为__________,溶液②中
c(Ba2+)为__________________。
③某同学取同样的溶液③和溶液④直接混合,则混合溶液的pH为__________(假设混合后溶液的体积为混合前两溶液的体积之和)。
参考答案:(1)BaSO4既不溶于水,也不溶于酸,可经人体排出体外,不会引起Ba2+中毒
(2)BaCO3遇到胃酸生成Ba2+会使人中毒,反应离子方程式为:BaCO3+2H+=Ba2++H2O+CO2↑
(3)①A;C;②5.5×10-10mol・L-1;2.2×10-10mol・L-1;③13
本题解析:
本题难度:一般
5、填空题 Al(OH)3为两性氢氧化物,在水溶液中存在酸式电离和碱式电离两种形式,试根据平衡移动反应物质,解释下列有关问题。
(1)向Al(OH)3沉淀中加入盐酸,沉淀溶解,其原因是_________________,有关离子方程式是___________________。
(2)向Al(OH)3沉淀中加入苛性钠溶液,沉淀溶解,其原因是__________________,有关离子方程式是______________________。
参考答案:(1)Al(OH)3的碱式电离为Al(OH)3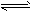 Al3++3OH-,加入盐酸溶液,由于H+与Al(OH)3电离出来的少量
Al3++3OH-,加入盐酸溶液,由于H+与Al(OH)3电离出来的少量
OH-中和生成水,使Al(OH)3的电离平衡向电离方向移动;Al(OH)3+3H+==Al3++3H2O
(2)Al(OH)3的酸式电离为Al(OH)3+H2O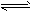 H++[Al(OH)4]-,当向Al(OH)3沉淀中加入碱溶液时,OH-与
H++[Al(OH)4]-,当向Al(OH)3沉淀中加入碱溶液时,OH-与
H+反应生成水,Al(OH)3的酸式电离平衡向正方向移动;Al(OH)3+OH-==[Al(OH)4]-
本题解析:
本题难度:一般