时间:2025-06-25 23:08:20
1、选择题 已知:1u(s)+2H+(aq)═1u2+(aq)+H2(g)△H1
2H2O2(l)═2H2O(l)+O2(g)△H2
2H2(g)+O2(g)═2H2O(l)△H4
则反应1u(s)+H2O2(l)+2H+(aq)=1u2+(aq)+2H2O(l)的△H是( ? )
A.△H=△H1+1/2△H2+1/2△H3
B.△H=△H1+1/2△H2-1/2△H3
C.△H=△H1+2△H2+2△H3
D.△H=2△H1+△H2+△H3
2、选择题 在298K、100kPa时,已知:2H2O(g) = 2H2(g) + O2(g) ΔH1; Cl2(g) + H2(g) = 2HCl(g) ΔH2
2Cl2(g) + 2H2O(g) = 4HCl(g) + O2(g) ΔH3; 则ΔH3与ΔH1和ΔH2间的关系正确的是
[? ]
A.ΔH3=ΔH1+2ΔH2
B.ΔH3=ΔH1+ΔH2
C.ΔH3=ΔH1-2ΔH2
D.ΔH3=ΔH1-ΔH2
3、填空题 能源是人类生存和发展的重要支柱。研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义。已知下列热化学方程式:
① 2H2(g)+O2(g)=2H2O(l) ;△H=-570kJ/mol;
② H2(g)+1/2O2(g)=H2O(g) ;△H=-242kJ/mol
③ C(s)+1/2O2(g)=CO(g) ;△H= -110.5kJ/moL
④ C(s)+O2(g)=CO2(g) ;△H=-393.5kJ/moL
⑤ CO2(g) +2H2O(g)=2CH4(g) +2O2(g);△H= +890kJ/moL
回答下列问题:
(1)上述反应中属于吸热反应的是____________________________
(2)H2的燃烧热为_______________。
(3)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然难直接测定,但可通过间接的方法求得。已知C(s) + H2O(g)= H2(g)+ CO (g) △H=akJ/moL;则a=________;该反应的熵△S_______0(选填“>”、“=”、“<”)。
4、选择题 灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn(s、白)+2HCl(aq)=SnCl2(aq)+H2(g) △H1
②Sn(s、灰)+2HCl(aq)=SnCl2(aq)+H2(g) △H2
③Sn(s、灰)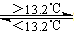 Sn(s、白) △H3=+2.1kJ/mol
Sn(s、白) △H3=+2.1kJ/mol
下列说法正确的是
[? ]
5、填空题 1840年盖斯根据一系列实验事实得出规律,他指出:“若是一个反应可以分步进行,则各步反应的反应热总和与这个反应一次发生时的反应热相同。”这是在各反应于相同条件下完成时的有关反应热的重要规律,称为盖斯定律。已知金刚石和石墨分别在氧气中完全燃烧的热化学方程式为:
C(金刚石、s)+O2(g)=CO2(g);△H=-395.41kJ/mol,
C(石墨、s)+O2(g)=CO2(g);△H=-393.51kJ/mol,
则金刚石转化石墨时的热化学方程式为:_____________________。由此看来更稳定的碳的同素异形体为:____________。若取金刚石和石墨混合晶体共1mol 在O2中完全燃烧,产生热量为QkJ,则金刚石和石墨的物质的量之比为_____________(用含Q的代数式表示)。