时间:2025-06-25 22:42:20
1、选择题 在水溶液中能大量共存的一组离子是(?)
A.HCO3-、H+、NO3-、Na+
B.Na+、Cu2+、OH-、SO42-
C.Mg2+、H+、AlO2-、SO42-
D.NH4+、K+、Br-、NO3-
2、选择题 某无色溶液,由Na+、K+、Ag+、Ba2+、Al3+、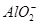 、
、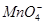 、
、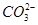 、
、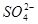 中的若干种组成。取该溶液进行如下实验:(1)取适量溶液,加入过量盐酸,有气体生成,并得到溶液;(2)在(1)所得溶液中加入过量的碳酸氢铵溶液,有气体生成,同时析出白色沉淀甲;(3)在(2)所得溶液中加入过量氢氧化钡溶液,微热,也有气体生成,同时析出白色沉淀乙。则下列离子在原溶液中一定存在的是(?)
中的若干种组成。取该溶液进行如下实验:(1)取适量溶液,加入过量盐酸,有气体生成,并得到溶液;(2)在(1)所得溶液中加入过量的碳酸氢铵溶液,有气体生成,同时析出白色沉淀甲;(3)在(2)所得溶液中加入过量氢氧化钡溶液,微热,也有气体生成,同时析出白色沉淀乙。则下列离子在原溶液中一定存在的是(?)
A.Na+
B.Al3+
C.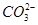
D.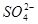
3、填空题 含有下列离子的五种溶液①Ag+ ②Mg2+ ③Al3+ ④ Fe2+ ⑤Fe3+ 试回答下列问题:
(1)既能被氧化又能被还原的离子是____________(填离子符号,下同)
(2)向④中加入NaOH溶液,现象是 有关化学方程式为
、 。
(3)加入过量NaOH溶液无沉淀的是_____________
(4)加铁粉溶液质量增重的是_________,溶液质量减轻的___________
(5)遇KSCN溶液呈红色的是_________________________
(6)能用来鉴别Cl
4、选择题 常温下,下列各组离子,在所给的条件下,一定能够大量共存的是(?)
A.在滴加酸碱指示剂酚酞试液后呈现红色的溶液中:Na+、Cl-、AlO2-、CO32-
B.在由水电离出的c(H+)=1×10-12mol/L的溶液中: HCO3-、Al3+、NH4+、ClO-
C.在c(H+)/c(OH-)=1×1012的溶液中:Fe2+、Mg2+、CO32-、NO3-
D.在AlCl3溶液中:K+、NO3-、S2-、Na+
5、选择题 无色透明的强碱性溶液中,能大量共存的一组是( )
A.Fe3+、Na+、NO3-、Cl-
B.K+、Ba2+、SO42-、NO3-
C.Na+、K+、CO32-、Cl-
D.Na+、Cu2+、SO42-、NO3-