时间:2025-06-25 22:39:45
1、选择题 下列与实验相关的叙述正确的是(? )
A.中和热测定实验时,如果没有环形玻璃棒,可用环形铜质搅拌棒代替
B.配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出
C.检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸
D.酸碱滴定时,若加入待测液前用待测液润洗锥形瓶,将导致测定结果偏高
参考答案:D
本题解析:
本题难度:简单
2、选择题 强酸与强碱的稀溶液发生中和反应的热效应为:H+(aq)+OH-(aq)=H2O(l) △H=-57.3KJ・mol-1。分别向1L 0.5mol・L-1的Ba(OH)2的溶液中加入①浓硫酸;②稀硝酸;③稀醋酸,恰好完全反应的热效应分别为
△H1、△H2、△H3,下列关系正确的是
[? ]
A.△H1>△H2>△H3
B.△H1<△H2<△H3
C.△H1>△H2=△H3
D.△H1=△H2<△H3
参考答案:B
本题解析:
本题难度:一般
3、填空题 在量热计(如下图所示)中将l00cm3、0. 500mol・L-1 CH3COOH溶液与100cm3、0. 500mol・L-1 NaOH溶液混合,温度从298.16K升高到300. 71K。已知量热计的热容常数(量热计各部件每升高1K所需的热量)是150. 5J・K-1,CH3COONa溶液比热容为4.03J・g-1・K-1,溶液的密度为0. 963g・cm-3。 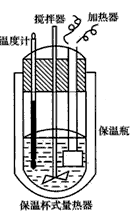
(1)试求CH3COOH的中和反应的反应热△H为____kJ・mol-1。
(2)CH3COOH的中和热的文献值为56. 1kJ・mol-1,请你分析(1)中测得的实验值偏差的可能原因是____。
(3)已知HCl( aq) +NaOH (aq)=NaCl(aq) +H2O(l) △H=- 57. 3kJ.mol-1;现有①CH3COOH、②浓H2SO4、
③HNO3与NaOH溶液反应的反应热分别为 △H1、△H2、△H3,则△H1、△H2、△H3三者的大小关系为___。
参考答案:(1)47.3
(2)CH3COOH的电离为吸热反应,且反应后生成的CH3COONa水解也要吸收热量
(3)△H1>△H3>△H2
本题解析:
本题难度:一般
4、选择题 下列说法正确的是( )
A.合成氨生产过程中高温、高压的反应条件,均可加快正反应速率,提高NH3的产率
B.硫酸工业中,为了提高SO3的吸收效率,在吸收塔内用稀H2SO4作吸收剂
C.测定中和反应的反应热,使用环形铜棒搅动溶液
D.为测定硫酸铜晶体里的结晶水含量,至少应进行四次称量
参考答案:D
本题解析:
本题难度:简单
5、选择题 下列实验装置图完全正确的是?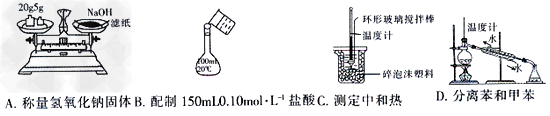
[? ]
A.称量氢氧化钠固体?
B.配制150mL0.10mol・L-1盐酸
C.测定中和热?
D.分离苯和甲苯
参考答案:C
本题解析:
本题难度:简单