时间:2025-06-25 22:34:50
1、选择题 向NaBr、NaI、Na2CO3的混合溶液中通入足量氯气后,将溶液蒸于并充分灼烧,得到固体剩余物的组成可能是?
A.NaCl
B.NaCl、NaHCO3
C.NaCl、I2
D.NaCl、NaI、Na2CO3
参考答案:A
本题解析:通入足量氯气后,反应生成NaCl、Br2、I2、CO2;加热灼烧过程中Br2、I2、CO2离开,最终只有NaCl。
本题难度:一般
2、实验题 已知Cl2和碱溶液在不同条件下,得到的产物不同。某兴趣小组用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。(3Cl2+6KOH KClO3+5KCl+3H2O )
KClO3+5KCl+3H2O )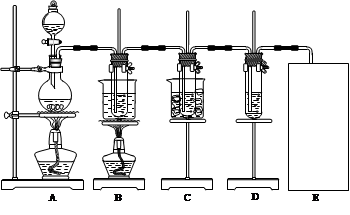
图中:A为氯气发生装置;B的试管里盛有15 mL 30% KOH溶液,并置于水浴中;C的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;D的试管里加有紫色石蕊试液。请填写下列空白:
(1)制取氯气时,在圆底烧瓶里加入一定质量的二氧化锰,通过?(填仪器名称)向圆底烧瓶中加入适量的浓盐酸。装置A中反应的离子方程式为?。需要向烧瓶中加碎瓷片吗??(选填:“需要”、“不需要”)。
(2)反应结束后,烧瓶里的溶液?。
A一定显酸性;B可能显酸性,也可能为中性;C只有氧化性;D只有还原性;E既有氧化性又有还原性
(3)反应完毕,B试管中有少量晶体析出,经冷却后,有大量晶体析出。图中符合该晶体溶解度曲线的是?(填编号字母);从B的试管中分离出该晶体必须用到的玻璃仪器有?。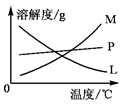
(4)该小组同学发现制得的氯酸钾产量偏低,可能的一种原因是Cl2中含有HCl气体。对此问题可以通过改进实验装置的方法进行避免。方法是?。
(5)实验中可观察到D的试管里溶液的颜色由紫色先变为_________色,最终变为________色。
(6)C装置中反应完毕的现象是______________________________________________。
(7)请在装置图方框中画出缺少的实验装置,并注明试剂。
参考答案:分液漏斗(1分);MnO2+4H++2Cl- Mn2++Cl2↑+2H2O(2分)(化学式错误、未配平无分。掉、错反应条件;掉、错关键箭头;等号用成箭头或可逆符号;合计扣1分。此标准下同)。不需要(1分)(所有选填,必须遵守试题说法,否则不给分,例如本空填“不”不给分。此标准下同)
Mn2++Cl2↑+2H2O(2分)(化学式错误、未配平无分。掉、错反应条件;掉、错关键箭头;等号用成箭头或可逆符号;合计扣1分。此标准下同)。不需要(1分)(所有选填,必须遵守试题说法,否则不给分,例如本空填“不”不给分。此标准下同)
(2)AE(2分)(全对得2分,对而不全得1分,其余不得分)
(3)M(1分);漏斗(或普通漏斗、三角漏斗)、玻璃棒(不能写为玻棒)、烧杯(或小烧杯)(1分)?(全对才能得1分)
(4)在A、B装置之间加一个盛饱和食盐水的试管(或洗气瓶、试剂瓶)(2分)(位置1分、试剂1分。独立采分。某点错,不影响另一点得分。位置:A后或B前不得分。试剂:饱和必须有,NaCl可以是其它溶解度较大的盐酸盐。)
(5)红(1分);无(1分) (6)C中试管上部空间充满黄绿色气体(1分,其他合理答案给分)
(7)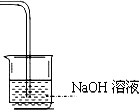 ①试剂为强碱溶液(浓度不作要求)(1分)。②导管要通入液面至少1/3,太浅不可 ③ 是一个敞口体系。(1分)(①和②③分开采分,彼此不牵连。②③错一条,则第2分不给。)
①试剂为强碱溶液(浓度不作要求)(1分)。②导管要通入液面至少1/3,太浅不可 ③ 是一个敞口体系。(1分)(①和②③分开采分,彼此不牵连。②③错一条,则第2分不给。)
本题解析:(1)向烧瓶中加热浓盐酸,需要借助于分液漏斗。在加热的条件下二氧化锰氧化浓盐酸生成氯气,反应的离子方程式为MnO2+4H++2Cl- Mn2++Cl2↑+2H2O;由于在反应中二氧化锰不溶于水,以固体的形式存在,因此反应中不需要再加热碎瓷片。
Mn2++Cl2↑+2H2O;由于在反应中二氧化锰不溶于水,以固体的形式存在,因此反应中不需要再加热碎瓷片。
(2)由于在反应过程中浓盐酸的浓度逐渐降低,而二氧化锰不能氧化稀盐酸,所以反应结束后盐酸一定剩余,溶液显酸性。同时反应中还生成氯化锰具有还原性。而溶液中的氢离子还具有氧化性,所以答案选AE。
(3)冷却后有大量晶体析出,这说明该物质的溶解度受温度的影响较大。且溶解度随温度的升高而增大,所以符合条件的曲线是M。从溶液中分离出固体的操作是过滤,需要的玻璃仪器有漏斗、玻璃棒、烧杯。
(4)由于氯化氢极易溶于水,氯气在水中的溶解度较小,所以要除去氯气中的氯化氢气体,可以通入到盛有饱和食盐水的洗气瓶中,即正确做法是在A、B装置之间加一个盛饱和食盐水的洗气瓶。
(5)氯气溶于水生成盐酸与次氯酸。溶液显酸性,则石蕊试液变为红色。又因为次氯酸还具有强氧化性,能漂白酸碱指示剂,因此溶液最终变为无色。
(6)在冰水浴中氯气与氢氧化钠溶液的反应很慢,且氯气在水中的溶解度很小,所以C装置中反应完毕的现象是C中试管上部空间充满黄绿色气体。
(7)氯气有毒,需要尾气处理,一般用氢氧化钠溶液吸收,则实验装置图为 。
。
本题难度:一般
3、选择题 要制取纯净气体,必须根据气体的逸出环境分析可能含有的杂质,再根据气体本身和杂质的性质决定除杂方案。干燥是除去水蒸气的一种除杂方法,下列不能用来干燥氯气的干燥剂是(? )
A.浓硫酸
B.五氧化二磷
C.无水氯化钙
D.生石灰
参考答案:D
本题解析:生石灰为氧化钙,属于碱性氧化物,能与氯气反应,不能用来干燥氯气;
本题难度:简单
4、填空题 (12分)下列框图中的A―J是中学化学中常见的八种物质,所有物质均由短周期元素组成,已知常温、常压下D为无色液体, C、E、G均为气体单质,B为金属,I是由3个原子组成的一元含氧弱酸分子, A―J可发生如下转化: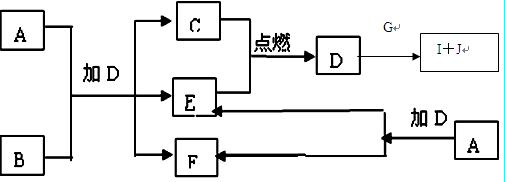
请填写下列空白:
⑴G的名称为?,F的电子式为?。
⑵15.6gA与D完全反应,转移的电子的物质的量为?。
⑶常温下,A为一种?色的固体,它的一种重要用途是? ?。
?。
⑷写出D、G反应转化为I和J的离子方 程式?
程式? ?。
?。
参考答案:
本题解析:略
本题难度:困难
5、选择题 生活中难免会遇到一些突发事件,我们要善于利用学过的知识,采取科学、有效的方法保护自己。如果发生了氯气泄漏,以下自救方法得当的是
[? ]
A.只要在室内放一盆水
B.向地势低的地方撤离
C.观察风向,顺风撤离
D.用湿毛巾或蘸有石灰水的毛巾捂住口鼻撤离
参考答案:D
本题解析:
本题难度:简单