时间:2025-06-25 22:27:36
1、实验题 (10分)我省 自贡盛产食盐,人类与食盐关系密切,食盐在老百姓生活和现代社会的工农业生产中均有重要作用,没有食盐的生活是不可以想象的。粗盐中含有Ca2+、Mg2+、SO42-以及泥沙等杂质,
自贡盛产食盐,人类与食盐关系密切,食盐在老百姓生活和现代社会的工农业生产中均有重要作用,没有食盐的生活是不可以想象的。粗盐中含有Ca2+、Mg2+、SO42-以及泥沙等杂质,
(1)为了除去粗盐中的泥沙,可采用的实验操作方法的名称是____▲____
(2)为了除去可溶性杂质,可以按以下实验步骤进行提纯:①加过量BaCl2溶液;②加过量NaOH溶液;③加过量Na2CO3溶液;④过滤;⑤加适量盐酸。
其中,在步骤③中涉及的离子反应方程式有___?▲?; ?▲?。?
(3)含碘食盐往往加入KIO3,为了检验实验中是否含KIO3,可以用以下反应进行:
KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O
为了从反应后的溶液中提取得到纯净的I 2,可采用的实验操作方法的名称是___▲__?。
2,可采用的实验操作方法的名称是___▲__?。
参考答案: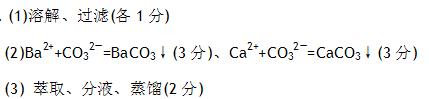
本题解析:略
本题难度:一般
2、选择题 下列溶液中含Cl-浓度最大的是
A.10mL0.1mol/L的AlCl3溶液
B.20mL0.1mol/LCaCl2溶液
C.30mL0.2mol/L的KCl溶液
D.100mL0.25mol/L的NaCl溶液
参考答案:A
本题解析:分析:溶液中不水解的离子的物质的量浓度=溶质的物质的量浓度×化学式中离子的个数,与溶液的体积无关,据此分析解答.
解答:A、10mL 0.1mol/L 的AlCl3溶液中氯离子的物质的量浓度=0.1mol/L×3=0.3 mol/L;
B、20mL0.1mol/LCaCl2溶液中氯离子的物质的量浓度=0.1mol/L×2=0.2mol/L;
C、30mL0.2mol/L的KCl溶液中氯离子的物质的量浓度=0.2mol/L×1=0.2mol/L;
D、100mL0.25mol/L的NaCl溶液中氯离子的物质的量浓度=0.25mol/L×1=0.25mol/L;
故选A.
点评:明确“溶液中不水解的离子的物质的量浓度=溶质的物质的量浓度×化学式中离子的个数,与溶液的体积无关,”是解本题的关键,难度不大.
本题难度:困难
3、选择题 下列有关物质检验的实验结论正确的是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| B | 向某溶液中加入2滴KSCN溶液,溶液不显红色。再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
| C | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊 | 该溶液中一定有CO32- |
| D | 用洁净的铂丝蘸取某溶液,在无色火焰上灼烧,观察到火焰颜色为黄色 | 该溶液中一定含有Na+,可能含有K+ |
参考答案:BD
本题解析:A、向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成,原溶液中可能含有Ag+、SO42-等,都可以生成白色沉淀,错误;B.向某溶液中加入2滴KSCN溶液,溶液不显红色,说明不含三价铁离子,再向溶液中加入几滴新制的氯水,溶液变为红色,说明生成了三价铁离子,证明溶液中一定含有亚铁离子,正确;C、加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,溶液中可能含有碳酸根、碳酸氢根等,错误;D、用洁净的铂丝蘸取某溶液,在无色火焰上灼烧,观察到火焰颜色为黄色,该溶液中一定含有Na+,可能含有K+,正确。
本题难度:一般
4、选择题 仅用一种试剂鉴别苯酚溶液、己烷、己烯、乙醇4种物质,可选用的是
A.浓溴水
B.FeCl3溶液
C.蒸馏水
D.NaOH溶液
参考答案:A
本题解析:浓溴水和苯酚反应生成白色沉淀,和己烷发生萃取,和己烯发生加成反应,和乙醇互溶,可以鉴别,A正确;氯化铁溶液只能鉴别苯酚和乙醇,不能鉴别己烷和己烯,B不正确;蒸馏水不能鉴别己烷和己烯,C不正确。氢氧化钠溶液和己烷、己烯均不反应,混合后分层,和乙醇互溶,和苯酚反应没有明显的现象,无法鉴别,答案选A。
点评:进行物质的检验和鉴别时,要依据物质的特殊性质和特征反应,选择适当的试剂和方法,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理、验证即可。如果是有机物,则需要依据官能团性质的不同进行鉴别。
本题难度:一般
5、选择题 现有一瓶物质甲和乙的混合物,已知甲和乙的某些性质如下表。
| 物质 | 分子式 | 熔点/℃ | 沸点/℃ | 密度/ g・cm-3 | 水中 溶解性 |
| 甲 | C3H6O2 | -98 | 57.5 | 0.93 | 可溶 |
| 乙 | C4H8O2 | -84 | 107 | 0.98 | 可溶 |
参考答案:C
本题解析:略
本题难度:一般