时间:2021-06-11 07:07:58
1、简答题 下图是甲、乙、丙三名同学设计的验证铜和浓硝酸反应原理的装置
已知:2NO2+2NaOH═NaNO3+NaNO2+H2O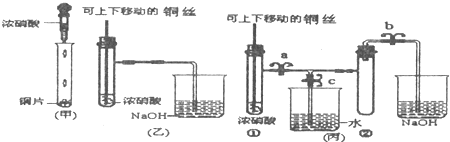
(1)写出铜和浓硝酸反应的离子反应方程式是______.
(2)和甲同学装置相比,乙同学设计的装置的优点是______、______.
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置.
先关闭弹簧夹______(填a或b或c),再打开弹簧夹______和______(填a或b或c),才能使NO2气体充满②试管.
(4)当气体充满②试管后,将铜丝提起与溶液脱离,欲使烧杯中的水进入②试管.应如何操作______.
(5)某位同学的实验中未得到蓝色的溶液,而呈绿色,他分析可能是生成的部分NO2溶解在溶液中造成的.请你帮他设计简单实验方案验证他的推测.
2、选择题 下列制备和收集气体的实验装置合理的是 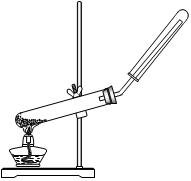
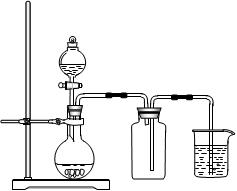
A.用氯化铵和氢氧化钙制NH3
B.用铜片和稀硝酸制NO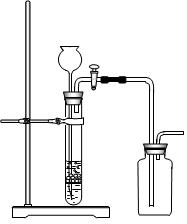
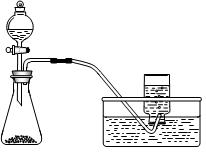
C.用锌粒和稀硫酸制H2
D.用双氧水和二氧化锰制O2
3、简答题 碘酸钾是一种白色结晶粉末,无臭无味,酸性条件下碘酸钾是一种较强的氧化剂,与氢碘酸、二氧化硫等还原性物质作用,被还原为单质碘,在碱性介质中,碘酸钾能被氯气、次氯酸盐等氧化为高碘酸钾.碘酸钾在常温下稳定,加热至560℃开始分解.工业生产碘酸钾的流程如下,在反应器中发生反应的化学方程式为:I2+KClO3+H2O--KH(IO3)2+KCl+Cl2↑(未配平)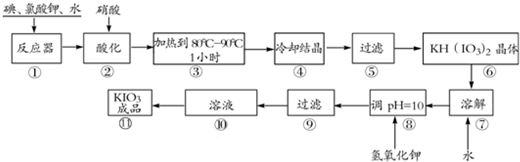
(1)已知步骤①反应器发生的反应中,两种还原产物所得电子数相同,请配平该反应的化学方程式:______;
(2)步骤②中,用稀酸酸化的作用是______;不能选用稀盐酸的原因是______;
(3)步骤③要保持溶液微沸1小时以完全排出氯气,排出氯气的原因为______;
(4)参照下表碘酸钾的溶解度,步骤11得到碘酸钾晶体,你建议的方法是______.
温度/℃
4、实验题 (14分)有一化学样品Na2SO3,可能含有NaCl、Na2SO4、KNO3、K2CO2、K2SO4中的一种或几种杂质,某实验小组利用图12提供的装置确定该样品的成分及Na2SO3的质量分数。称此样品6.30g,加入6.0mol·L-1的硫酸至过量,产生无色气体560mL(标准状况),向逸出气体后的溶液中加入稍过量的BaCl2溶液,得到白色沉淀9.32g,透过蓝色钻玻璃观察,滤液的焰色反应无紫色。请回答下列问题: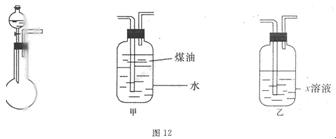
(1)溶液X是?,煤油的作用是?。
(2)若实验中加入硫酸溶液的体积为5.00mL,则样品中Na2SO3的质量分数是?,
写出有关离子方程式?。
(3)结合已提供的实验仪器,设计实验(实验仪器自选)如何正确测出气体的体积,简述操作步骤:??
?。
(4)说明一定含有硫酸钠的依据:??
? ?。
?。
5、简答题 某研究性学习小组通过实验来探究乙二酸(又名草酸)受热分解的产物,他们设计的实验装置如图所示: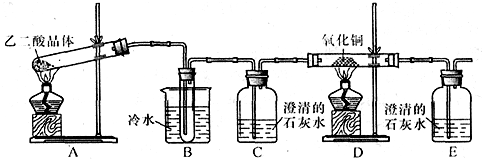
查阅资料可知:乙二酸晶体(H2C2O4?2H2O)熔点100.1℃,草酸钙是难溶于水的白色固体;Cu2O能溶于稀硫酸,立即发生歧化反应生成Cu2+和Cu.
(1)实验过程中观察到C、E装置中的溶液均变浑浊,且D装置中黑色粉末变为红色,写出A中发生反应的化学方程式:______;
(2)装置B的作用是______;上述装置中有两处需要改进(假设洗气装置每次吸收气体均完全),改进方法是______;______.
(3)实验结束后向装置B的试管中加入NaHCO3溶液,产生大量无色气体,由此可以证明两种物质的酸性强弱顺序是______.
(4)有人认为D装置中得到的红色固体可能是Cu,也可能是Cu和Cu2O的混合物.实验小组进一步探究:①取少量红色固体加入到盛稀硫酸的试管中,充分振荡,溶液变为蓝色,试管底部仍有红色固体,由此可以得出的结论是______.②取6.8g红色固体与足量的稀硝酸反应,收集到标准状况下的NO气体1.12L.则红色固体中含单质铜的质量分数是______.