时间:2021-06-11 07:05:40
1、填空题 (12分)⑴第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为? ▲?。在GaN晶体中,与同一个Ga原子相连的N原子构成的空间构型为? ▲?。在四大晶体类型中,GaN属于? ▲?晶体。
⑵铜、铁元素能形成多种配合物。微粒间形成配位键的条件是:一方是能够提供孤电子对的原子或离子,另一方是具有? ▲?的原子或离子
⑶CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子:请回答下列问题: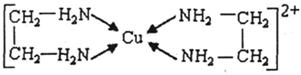
① H、N、O三种元素的电负性由大到小的顺序是? ▲?。
②SO2分子的空间构型为? ▲ 。与SnCl4互为等电子体的一种离子的化学式为? ▲
③乙二胺分子中氮原子轨道的杂化类型为? ▲?。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是? ▲?。
④⑶中所形成的配离子中含有的化学键类型有? ▲?。
a.配位键? b.极性键? c.离子键? d.非极性键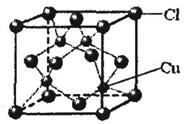
⑤CuCl的晶胞结构如上图所示,其中Cl原子的配位数为? ▲?。
参考答案:(12分)
⑴1s22s22p63s23p63d104s24p1(或[Ar]3d104s24p1)(1分)
正四面体(1分)原子晶体(1分)
⑵能够接受孤电子对的空轨道(1分)
⑶①?O >N >H(1分)
②V形(1分)? SO42-、SiO44-等(1分)
③sp3杂化(1分)?乙二胺分子间可以形成氢键,三甲胺分子间不能形成氢键(1分)
④abd?(2分)?⑤4(1分)
本题解析:略
本题难度:简单
2、选择题 石墨能与熔融金属钾作用,形成石墨间隙化合物,K原子填充在石墨各层碳原子中,比较常见的石墨间隙化合物是青铜色的化合物,其化学式可写作CxK,平面结构如图所示.则x值为( )
A.8
B.12
C.24
D.60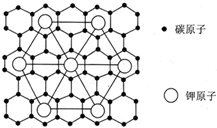
参考答案:A
本题解析:
本题难度:简单
3、选择题 金属的下列性质中,不能用电子气理论加以解释的是( )
A.易导电
B.易导热
C.有延展性
D.易锈蚀
参考答案:D
本题解析:金属易锈蚀,是因为在反应中易失去最外层电子,具有较强的还原性。
本题难度:简单
4、填空题 某离子晶体晶胞如图所示,阳离子 X(●)位于立方体的顶点, 阴离子Y(○)位于立方体的中心,试分析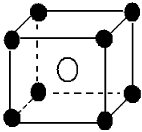
(1)晶体中Y的配位数是___________; X的配位数是___________;该晶体的化学式为___________。
(2)晶体中在每个X周围与它最接近且距离相等的X共有___________个。
(3)该晶体的摩尔质量为Mg/mol,晶体密度为ρg/cm3,阿伏加德罗常数为NA,则晶体中两个距离最近的X中心间的距离为___________cm。
参考答案:(1)8;8;XY
(2)6
(3)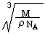
本题解析:
本题难度:一般
5、计算题 下图是超导化合物----钙钛矿晶体中最小重复单元(晶胞)的结构。请回答: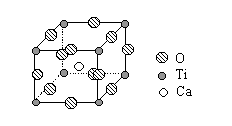
(1)该化合物的化学式为?。
(2)在该化合物晶体中,与某个钛离子距离最近且相等的其他钛离子共有?个。
(3)设该化合物的式量为M,密度为ag/cm3,阿伏加德罗常数为NA,则晶体中钙离子与钛离子之间的最短距离为?。
参考答案:(1) CaTiO3?(2)6? (3)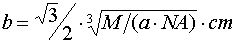
本题解析:(1)这个晶胞对位于顶点上的每个钛原子占有的份额为1/8,所以,它单独占有的钛原子个数为8×1/8=1个;它对位于棱上的每个氧原子占有的份额为1/4,所以,它单独占有的氧原子个数为12×1/4=3个;它全部拥有体内的那一个钙原子,所以,该晶胞中单独占有的钛原子、氧原子和钙原子的个数分别为:1、3、1;所以,该化合物的化学式为CaTiO3。
(2)钛位于立方体的顶点上,与一个钛离子距离最近的钛离子是与它共棱的。从上面立方晶胞进行堆积的图2和图3可以看出,在X轴或Y轴或Z轴上,与它共棱的离子都是二个,所以,共6个。
(3)这是个综合性较大的习题。设这种立方晶胞的边长是b,那么,钙离子与钛离子之间
的距离是体对角线的一半,即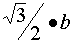 。
。
下面求b。因为每个立方体的体积为b3,而NA个这样的立方体堆积到一起就是1mol晶体,其质量为Mg,其体积为Mg/ag/cm3="M/a" cm3。所以,NA·b3="M/a" cm3,所以,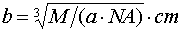 ,
,
所以,题中所求距离为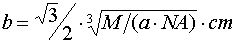 。
。
本题难度:一般