1、选择题 为了除去粗盐中的Ca2+,Mg2+,SO42-及泥沙,得到纯净的NaCl,可将粗盐溶于水,然后在下列操作中选取必要的步骤和正确的操作顺序 ①过滤; ②加过量NaOH溶液; ③加过量盐酸; ④加过量NaCO3溶液; ⑤加过量
BaCl2溶液
[? ]
A.④②⑤
B.②⑤④①③
C.④①②⑤③
D.①④②⑤③
2、选择题 下列说法正确的是
A.实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液
B.氨基酸是人体必需的营养物质,其晶体主要以内盐形式存在,调节溶液的pH可改变它的溶解度
C.在苯酚和乙醇性质比较实验中,将等物质的量的乙醇和苯酚置于试管中,再投入金属钠,从而可以比较出羟基氢的活泼性
D.抽滤完毕,直接用玻璃棒刮下布氏漏斗中滤纸上的固体
3、选择题 下列实验操作或方法不能达到实验目的的是
[? ]
实验目的?
实验操作或方法
A.
分离苯和水?
分液
B.
从海水中提取淡水?
蒸馏
C.
提取碘水中的碘?
用酒精萃取
D.
分离硝酸钾和沙子
溶解后过滤
4、选择题 能够用来鉴别NH4Cl、NaCl、Na2CO3三种物质的试剂是(?)
A.AgNO3溶液
B.Ba(OH) 2溶液
C.稀盐酸
D.NaOH溶液
5、实验题 研究性学习小组对某硫酸亚铁晶体(FeSO4?xH2O)热分解研究,该小组同学称取ag硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行探究,并通过称量装置B质量测出x的值。
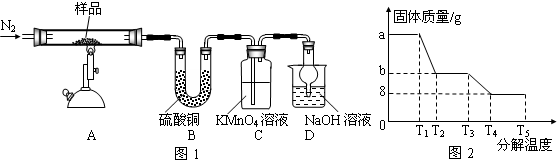
(1)装置B中硫酸铜粉末变蓝,质量增加12.6g,说明产物中有水,装置C中高锰酸钾溶液褪色,说明产物中还有??。
(2)实验中要持续通入氮气,否则测出的x会??(填“偏大”、“偏小”或“不变”)。
(3)硫酸亚铁晶体完全分解后装置A中还残留红棕色固体Fe2O3。
(4)从理论上分析得出硫酸亚铁分解还生成另一物质SO3,写出FeSO4分解的化学方程式??。
(5)装置D球形干燥管的作用??。
(6)某研究所利用SDTQ600热分析仪对硫酸亚铁晶体(FeSO4?xH2O)进行热分解,获得相关数据,绘制成固体质量――分解温度的关系图如图2,根据图2中有关数据,可计算出FeSO4?xH2O中的x=???。
微信搜索关注"91考试网"公众号,领30元,获取公务员事业编教师考试资料40G