时间:2021-06-11 06:20:08
1、选择题 “绿色化学”是当今社会提出的一个新概念。在“绿色化学工艺中,理想状态是反应物中原子全部转化为欲制的产物,即原子的利用率为100%。在用丙炔合成甲基丙烯酸甲酯
(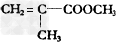 )的过程中,欲使原子利用率达到最高,还需要其他的反应物是
)的过程中,欲使原子利用率达到最高,还需要其他的反应物是
[? ]
A.CO和CH3OH?
B.CO2和H2O ?
C.H2和CO2?
D.CH3OH和H2
2、计算题 硫酸的工业制备是一个重要的化工生产过程,但同时在生产过程中会产生大量SO2等污染物。
(1)将SO2通入Fe(NO3)3溶液中,溶液由棕黄色变为浅绿色,但立即又变为棕黄色,此时若滴入BaCl2溶液,则会产生白色沉淀。溶液由棕黄色变为浅绿色用离子方程式表示为_____,后又由浅绿色变为棕黄色的离子方程式为_____。
(2)以硫酸工业的尾气、氨水、石灰石、焦炭及碳酸氢铵和KCI为原料可以合成有重要用途的硫化钙、硫酸钾、亚硫酸氢铵等物质。合成路线如下: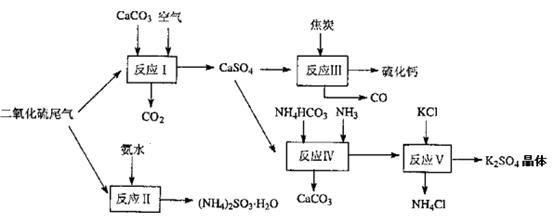
写出反应反应Ⅳ的化学方程式?;
反应III中氧化剂与还原剂的物质的量之比为__?__;
反应V在25"C、40%乙二醇溶液中进行,该复分解反应能顺利进行的原因是?。
(3)新型纳米材料氧缺位铁酸锌(ZnFe2Ox),常温下能使SO2分解,减小工业废气对环境的影响,它由铁酸锌(ZnFe2O4)经高温还原制得,转化流程如下图所示: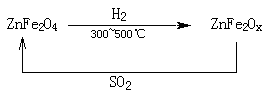
若2molZnFe2Ox与SO2反应可生成 0.75molS,x=?,写出铁酸锌高温下被还原生成氧缺位铁酸锌的化学方程式?
(4)石灰石-石膏湿法烟气脱硫工艺技术的原理是烟气中的二氧化硫与浆液中的碳酸钙以及空气反应生成石膏(CaSO4.2H2O),写出该反应的化学方程式?。某电厂用煤300t(煤中含硫的质量分数为2.5%),若燃烧时煤中的硫全部转化为二氧化硫,用该方法脱硫时有96%的硫转化为石膏,则可生产石膏?t。
3、选择题 工业上冶炼金属的方法正确的是
A.采用加热分解法冶炼金属钾
B.采用电解法冶炼金属铝和钠
C.采用热还原法冶炼金属铁与汞
D.采用热还原法冶炼金属铜与钙
4、选择题 下列措施符合“绿色化学”思想的是
[? ]
A.直接排放含磷生活污水
B.大量使用氟里昂作为冰箱制冷剂
C.使用可降解塑料代替不可降解塑料
D.使用化学性质稳定、不易分解的有机氯农药
5、选择题 “绿色化学”的最大特点在于它在始端就采用实现预防污染的科学手段,因而过程和终端均接近或达到零排放或零污染。“绿色食品”近来越来越受到人们的欢迎和重视。下列有关“绿色化学”及“绿色食品”的描述均正确的组合是
[? ]
①“绿色化学”是指绝对无污染的化学过程
②“绿色化学”是指依靠绿色植物来完成的化学过程
③“绿色化学”是没有或尽可能少污染的化学过程
④“绿色化学”是人们理想中的化学过程,无法实现
⑤治理工业 “三废”属于“绿色化学”范畴
⑥合理使用农药属于 “绿色化学”
⑦加强环境监测属于“绿色化学”过程
⑧开发利用氢能源属于“绿色化学”范畴
⑨富含叶绿素的食品
⑩新鲜的蔬菜无污染的安全、优质、营养类食品
贴有“绿色”防伪标志的食品
A.③⑧/
B.①②③⑤⑥⑧/⑩
C.②⑥⑦/⑨
D.④/