时间:2021-06-11 06:09:24
1、选择题 下列各组微粒不是等电子体的是
[? ]
A.N2.C22-
B.CO2.NO2
C.C6H6.B3N3H6
D.PCl3.NF3
参考答案:B
本题解析:
本题难度:简单
2、选择题 与NH4+互为等电子体的分子是( )
A.CH4
B.OH-
C.NH3
D.H3O+
参考答案:A
本题解析:
本题难度:一般
3、选择题 下列粒子属于等电子体的是
[? ]
A.CH4和NH4+
B.NO和O2
C.NH2-和H3O+
D.HCl和H2O
参考答案:A
本题解析:
本题难度:简单
4、简答题 三聚氰胺(结构简式如右)由于含氮量高而常被不法商人用作食品添加剂,因此三聚氰胺也被人称为“蛋白精”.三聚氰胺是一种纯白色晶体,无味,常压熔点354℃(分解);快速加热升华,升华温度300℃.三聚氰胺早期合成使用双氰胺法:由电石(CaC2)在N2氛围中加热可制备氰胺化钙(CaCN2),氰胺化钙水解后二聚生成双氰胺(C2H4N4),再加热即转化为三聚氰胺.与该法相比,尿素法成本低,目前较多采用.尿素以氨气为载体,硅胶为催化剂,在380-400℃温度下沸腾反应生成三聚氰胺:6CO(NH2)2→C3N6H6+6NH3+3CO2.
试回答下列问题:
(1)原子数和电子总数都相等的粒子互称为等电子体,它们具有相似的结构特征,与CN22-互为等电子体的中性分子有N2O和______(填化学式),由此可以推知CN22-离子的空间构型为______;
(2)写出由电石和N2在加热条件下反应制备氰胺化钙的化学方程式:______;若通过上述反应制备400g氰胺化钙,则转移的电子数为______mol;
(3)三聚氰胺难溶于冷水但易溶于热水,以尿素为原料制得的三聚氰胺粗产品中既含有不溶于水的杂质,又含有易溶于水的杂质,简述从粗产品中提纯三聚氰胺的方法:______
(4)在奶粉中掺入三聚氰胺后不易被发现的原因是______.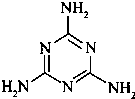
参考答案:(1)与CN22-互为等电子体的分子有N2O和CO2;等电子体具有相同的价电子数、原子总数,结构相似,二氧化碳分子是直线型,所以CN22-离子的空间构型是直线型.
故答案为:CO2;直线型;
(2)电石和N2在加热条件下反应制备氰胺化钙,化学方程式:CaC2+N2=CaCN2+C;由方程式可知生成1个CaCN2转移6个电子,制备400g(即5mol)氰胺化钙,则转移的电子数为30mol;
故答案为:CaC2+N2=CaCN2+C;30;
(3)三聚氰胺难溶于冷水但易溶于热水,可将将粗产品溶于热水中并趁热过滤,冷却待溶液中有大量晶体析出时再过滤,即可得三聚氰胺;
故答案为:将粗产品溶于热水中并趁热过滤,冷却待溶液中有大量晶体析出时再过滤;
(4)在奶粉中掺入三聚氰胺后不易被发现的原因是三聚氰胺为白色结晶粉末,没有什么气味和味道,
故答案为:三聚氰胺为白色结晶粉末,没有什么气味和味道.
本题解析:
本题难度:一般
5、选择题 根据等电子原理,下列分子或离子中与SO42-有相似结构的是
[? ]
A.PCl5
B.CCl4
C.F3
D.N2
参考答案:B
本题解析:
本题难度:简单