时间:2021-06-11 05:37:47
1、选择题 下列物质既含有非极性共价键又含有极性共价键的化合物是( ? )
A.Br2
B.CH4
C.NaOH
D.CH3COOH
参考答案:D
本题解析:
本题难度:一般
2、选择题 0.01 mol氯化铬(CrCl3· 6H2O)在水溶液中用过量AgNO3处理,产生0.02 mol AgCl沉淀,此氯化铬最可能为
?
A.[Cr(H2O)6]Cl3
B.[Cr(H2O)5Cl]Cl2·H2O
C.[Cr(H2O)4Cl2]Cl·2H2O
D.[Cr(H2O)3Cl3]·3H2O
参考答案:B
本题解析:假设0.01mol氯化铬中的氯离子全部能电离出来与银离子反应,那么将生成0.03mol AgCl.但题目结果只有0.02mol AgCl,说明了1 mol氯化铬中只有2mol氯离子能电离出来,其余的Cl元素无法电离,可能是以络合离子的形式存在,所以答案应选B.
本题难度:一般
3、选择题 二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂;其分子结构中每个原子均满足8电子结构。常温下,S2Cl2是一种橙黄色的液体,遇水易水解,并产生能使品红褪色的气体。下列说法中错误的是
A.S2Cl2中的硫元素显+1价
B.S2Cl2结构中的化学键只含有极性键
C.S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2
D.S2Cl2与H2O反应的生成物中可能有S
参考答案:B
本题解析:
S2Cl2的结构类似于H2O2的结构,为Cl-S-S-Cl,其中的S-S为非极性键,S-Cl键为极性键,由于分子中的4个原子不在同一直线上,共价键的极性不能相互抵消,所以S2Cl2是极性分子。B错误。
本题难度:简单
4、选择题 下列表述正确的是
[? ]
A.金刚石与12C互为同位素
B.NH3是由非极性键构成的
C.Na+的结构示意图: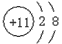
D.CCl4的电子式为: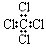
参考答案:C
本题解析:
本题难度:简单
5、选择题 aA、bB、cC、dD、eE五种短周期元素,它们的原子序数有如下关系:c-b=b-a=1且b+c=d,常见化合物E2C2与水反应生成C的单质,且溶液使酚酞试液变红.B的最高价氧化物对应水化物为强酸.下列说法正确的是( )
A.B与D形成的单质分别为甲、乙,非金属性:B>D,活泼性:乙>甲
B.1molE2C2与足量水完全反应生成C的单质,共转移电子2mol
C.原子半径:D>E>A>B>C
D.C的氢化物的沸点低于B的氢化物的沸点
参考答案:aA、bB、cC、dD、eE五种短周期元素,常见化合物E2C2与水反应生成C的单质,且溶液使酚酞试液变红,为过氧化钠与水反应生成氢氧化钠与氧气,故E为Na元素,C为O元素,原子序数:c-b=b-a=1,B的原子序数为7,A的原子序数为6,故B为N元素,A为C元素,由于b+c=d,D的原子序数为7+8=15,故D为P元素,
A、同主族自上而下非金属性减弱,故非金属性N>P,氮气的分子中为N≡N三键,键能很大,化学性质活泼,故活泼性乙>甲,故A正确;
B、1molNa2O2与足量水完全反应生成O2,反应中过氧化钠是氧化剂又是还原剂,各占一半,起还原剂作用的过氧化钠,氧元素化合价由-1价升高为0价,故转移电子为1mol,故B错误;
C、同周期自左而右,原子半径减小,同主族自上而下原子半径增大,故原子半径Na>P>C>N>O,即E>D>A>B>C,故C错误;
D、水常温下为液体,氨气常温下为气体,故水的沸点更高,故D错误;
故选A.
本题解析:
本题难度:一般