时间:2021-02-18 07:24:50
1、实验题 如下图所示,将浸透了石蜡油(17 个碳以上的液态烷烃混合物)的矿渣棉放在硬质玻璃管的底部,试管中加入碎瓷片,给碎瓷片加强热,石蜡油蒸汽通过炽热的碎瓷片表面发生反应。?
(1)若将生成的气体通入酸性高锰酸钾溶液后,溶液褪色并且液体分为两层,上层无色、油状,下层无色、水状。 ?
(2)若将生成的气体通入溴水,溴水也褪色。 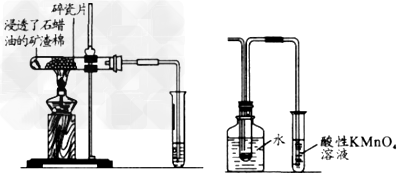
请回答下列问题: ?
(1)实验装置中矿渣棉的作用是____________,碎瓷片的作用是________。 ?
(2)酸性高锰酸钾溶液褪色,有机化合物发生的化学反应的类型是________。 ?
(3)溴水褪色,有机化合物发生的化学反应的类型是________,还能观察到的其他现象是
____________________。 ?
(4)若将生成的气体用上图所示的装置进行收集、检验,浸入水中的试管里形成了油状液体,另一试管内的酸性高锰酸钾溶液褪色。按上图所示的方法进行石蜡油裂化的实验,从实验安全性的角度来说,该实验设计中存在的主要问题是________________。 ?
(5)假设石蜡油中的某种烃的化学式是C18H38,它发生裂化反应生成了癸烷和烃A,癸烷又发生裂化反应生成了己烷和烃B,己烷又发生裂化反应生成了丁烷和烃C。写出上述裂化反应的化学方程式(有机化合物用化学式表示)。
①________________;②________________;③___________________。
2、填空题 (16分)卤块的主要成分是MgCl2,此外还含有少量的Fe3+、Fe2+和Mn2+等离子。以卤块为原料制取轻质氧化镁工艺以及相关数据如下:
常温下生成氢氧化物沉淀的pH数据:
| 物?质 | 开始沉淀时的pH | 沉淀完全时的pH |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
3、实验题 (10分)已知浓硫酸和木炭粉在加热条件下可发生化学反应。
(1)上述反应的化学方程式为?。
(2)试用下图所列各装置设计一个实验,来验证上述反应所产生的各种产物。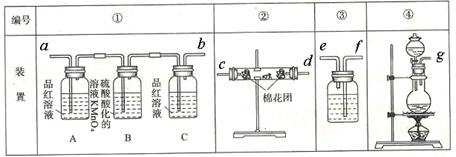
实验时可观察到装置①中A瓶中的溶液退色,C瓶中的溶液不退色。A瓶中的溶液的作用是
?;B瓶中的溶液的作用是?;C瓶中的溶液的作用是?。
(3)装置②中所加固体药品是无水硫酸铜。可验证的产物是?。
(4)装置③中所盛溶液是澄清石灰水,可验证的产物是?。
4、选择题 用标准浓度的盐酸滴定未知浓度的NaOH溶液,下列各操作(其他操作正确)中会造成测定结果偏低的是
A.酸式滴定管尖嘴部分有气泡,滴定后消失
B.滴定终点读数时俯视读数
C.用蒸馏水洗净酸式滴定管后,装入标准盐酸进行滴定
D.锥形瓶水洗后未干燥
5、简答题 化学实验是科学探究的基础.请回答有关实验问题:
(1)下面的四个实验装置有三个都存在明显缺陷,其中完全正确的是______: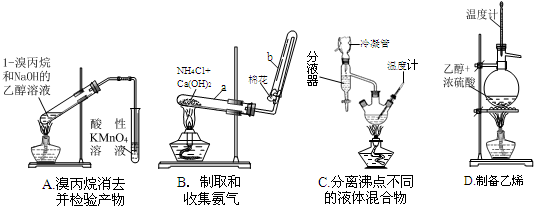
(2)要检验上面B装置氨气已集满的操作是______则试管已集满.
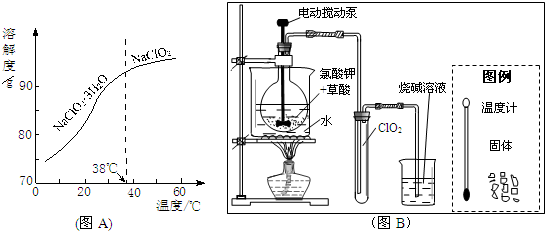
(3)ClO2是一种安全、高效、广谱、强力杀菌剂,其性质如表:
| 色态 | 溶于碱 | 超过1Kpa、受热或遇光 常温气体 -59-11℃ 红黄色液体 生成亚氯酸盐和氯酸盐 爆炸 | |