时间:2021-02-18 07:24:50
1、实验题 (18分)某中学化学课外活动小组欲探究铁在氯气中燃烧产物的成份、性质和用途,设计了如下实验步骤:
Ⅰ、用下列实验装置制取纯净干燥的氯气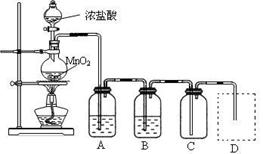
写出A、B中所盛放最佳化学试剂的名称?、?,画出虚线框内所需装置图并标明所需试剂的名称。
Ⅱ、某同学将一定量铁粉与Cl2恰好完全反应得到一固体物质a,然后通过实验确定其成分。探究过程如下:
(1)提出假设:(请把下列假设补充完整)
假设①:该固体物质是FeCl3;假设②:?;假设③:?。
(2)设计实验方案:
取少量固体物质a于烧杯中,加适量水溶解,然后取两份a溶液分别进行实验,实验现象与结论如下表,请在表格内的横线处填空。
| ?实验方法 | 实验现象 | 结论 |
| 在溶液中加 KSCN溶液 | ? | 固体物质中有FeCl3 |
| 向a溶液中滴加 酸性KMnO4溶液 | KMnO4溶液紫色 不褪色 | 固体物质中不含______ |
参考答案:(共18分)
Ⅰ、饱和食盐水(1分);浓硫酸(1分);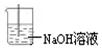 其它合理装置也对(2分)
其它合理装置也对(2分)
Ⅱ、(1)FeCl2(1分);FeCl3和FeCl2的混合物(1分)
(2)
实验方法
实验现象
结论
在溶液中加
KSCN溶液
溶液为红色(1分)?
固体物质中有FeCl3
向a溶液中滴加
酸性KMnO4溶液
KMnO4溶液紫色
不褪色
固体物质中不含FeCl2(1分)
本题解析:略
本题难度:一般
2、实验题 “化学是以实验为基础的科学”。在实验中感知化学知识是学好化学的关键。请针对以下实验回答问题:
(1)【实验一】室温下,将a?g?Ba(OH)2・8H2O粉末和a/2?g?NH4Cl粉末置于锥形瓶中,并将锥形瓶置于滴有几滴水的玻璃片上,迅速搅拌,然后用带有玻璃导管的单孔橡胶塞塞紧瓶口,如下图所示。 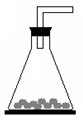
①该实验的现象是_________________。
②若将锥形瓶内物质加热产生的气体通入AlCl3溶液中,可观察到有白色沉淀生成,反应的离子方程式是________;分离出纯净的白色沉淀的主要操作有___________。
(2)【实验二】如下图所示,将适量的蔗糖放入小烧杯中,滴入几滴水,搅拌均匀。然后加入适量浓硫酸,迅速搅拌。反应放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀。 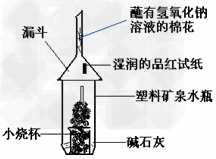
①蔗糖逐渐变黑,体现了浓硫酸的__________?性。
②湿润的品红试纸产生的现象是_________,产生该现象的物质是____________?,产生这一物质的化学方程式是___________,其中浓硫酸的作用是_____________。
④蘸有氢氧化钠溶液的棉花的作用是________________,发生反应的离子方程式是________________________。
(3)【实验三】如下图所示,将稀硝酸放入U型管中,把一端弯成螺旋状的Cu丝插到胶塞上。关闭分液漏斗活塞,塞好胶塞。 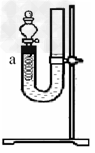
①反应一段时间后,可以看到a处液面下降,其他现象还有__________________。
②a处反应的离子方程式为_____________________?。
③检验a处产生气体的操作是_______________,现象和结论是________________?。
参考答案:(1)①锥形瓶壁变凉,玻璃片与锥形瓶粘在一起,有刺激性气味气体放出;②Al3++3NH3・H2O?=?Al(OH)3↓+3NH4+;过滤、洗涤、干燥
(2)①脱水;(2)湿润的品红试纸褪色;SO2;C+2H2SO4(浓)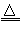 CO2↑+?2SO2↑+2H2O;强氧化剂;③吸收SO2,防止污染空气;?SO2?+2OH-=?SO32-+H2O
CO2↑+?2SO2↑+2H2O;强氧化剂;③吸收SO2,防止污染空气;?SO2?+2OH-=?SO32-+H2O
(3)①有无色气体生成,溶液变为蓝色;②3Cu?+?8H+?+?2NO3-?==?3Cu2+?+?2NO↑?+?4H2O;
③打开分液漏斗活塞;无色气体变为红棕色,说明该无色气体是NO。
本题解析:
本题难度:一般
3、实验题 氢化钙固体是登山运动员常用的能源提供剂。某兴趣小组长拟选用如下装置制备氢化钙。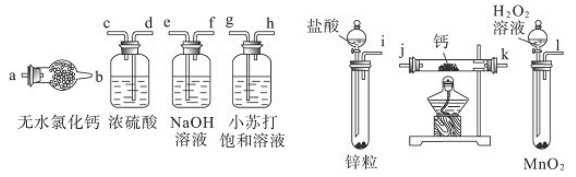
请回答下列问题:
(1)请选择必要的装置,按气流方向连接顺序为________(填仪器接口的字母编号)
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗活塞_________(请按正确的顺序填入下列步骤的标号)。
A.加热反应一段时间
B.收集气体并检验其纯度
C.关闭分液漏斗活塞
D.停止加热,充分冷却
(3)实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,溶液中加入酚酞后显红色,该同学据此断,上述实验确有CaH2生成。
① 写出CaH2与水反应的化学方程式 ___________________
②该同学的判断不正确,原因是_________________
(4)请你设计一个实验,用化学方法区分钙与氢化钙,写出实验简要步骤及观察到的现象___________。
(5)登山运动员常用氢化钙作为能源提供剂,与氢气相比,其优点是____________。
参考答案:
本题解析:略
本题难度:一般
4、选择题 利用下列试剂,选用合适方法鉴别Na2SO4、Na2SO3、Na2CO3、NaCl四种溶液,最佳试剂组是( )
A.BaCl2、HCl、石蕊溶液
B.BaCl2、HCl、品红溶液
C.AgNO3和HNO3溶液
D.AgNO3和BaCl2溶液
参考答案:A.加入BaCl2溶液分别生成BaSO4、BaSO3、BaCO3沉淀,BaSO3和BaCO3溶于盐酸,并且BaSO3与盐酸反应生成刺激性气味的SO2气体,而BaCO3与盐酸反应无色无味的CO2,SO2和CO2都能是石蕊试液变红,鉴别效果不好,故A错误;
B.在Na2SO4、Na2SO3、Na2CO3、NaCl中滴加BaCl2和HCl.Na2SO4生成沉淀不溶解;NaCl不生成沉淀;Na2SO3、Na2CO3生成沉淀后都溶解,但Na2SO3生成的气体可以使品红褪色,而Na2CO3不能,可鉴别,故B正确;
C.加入AgNO3和HNO3溶液,Na2SO3被氧化为Na2SO4,不能鉴别,故C错误;
D.加入AgNO3和BaCl2溶液,都生成白色沉淀,不能鉴别,故D错误.
故选B.
本题解析:
本题难度:简单
5、填空题 实验室有NH4HCO3和NaHSO3的干燥粉状混合物,某兴趣小组为测定其中NH4HCO3的含量,设计了用在混合物中加酸的实验方法来测定其质量分数。化学小组主要选用了下列药品和仪器进行实验(铁架台等固定仪器未画出)。按气流由左向右的方向,仪器连接顺序是 。回答以下问题:
。回答以下问题:
(1)A中加入硫酸溶液的仪器名称是:?。
(2)实验开始,混合物加酸前,A装置需要鼓入空气,排除装置中原有的空气。加酸后A装置再次鼓入空气的作用是? ?。
(3)E装置的作用是? ?。
(4)实验中,要确保实验中C瓶溶液不褪色,若C瓶中溶液褪色,则测定结果可能会偏? ?(填“高”或“低”)。
(5)若混合物样品质量为13.1g,充分作用后碱石灰增重4.4g,则混合物中NH4HCO3的质量分数为? ?。
(6)从定量测定的准确性考虑,该套装置还应作进一步的改进是?。
参考答案:(12分)(1)分液漏斗(2分)
(2)将生成的气体全部送入后续装置(使反应产生的SO2和CO2被完全吸收)(2分)
(3)除去SO2,以防止SO2对测定结果的影响(2分)
(4)高? (共2分)?(5)60.3%(2分)
(6)在B之后再接一个阻止空气中水蒸气和二氧化碳进入B的装置。(2分)
本题解析:(1)根据仪器的构造特点可知,A中加入硫酸溶液的仪器名称是分液漏斗。
(2)加酸后生成CO2和SO2气体,所以加酸后A装置再次鼓入空气的作用是将生成的气体全部送入后续装置(使反应产生的SO2和CO2被完全吸收)。
(3)由于SO2也能碱石灰吸收,会干扰CO2的测定,所以高锰酸钾溶液的作用是除去SO2,以防止SO2对测定结果的影响。
(4)若C瓶中溶液褪色,说明SO没有完全被除尽,也被碱石灰吸收,则测定结果可能会偏高。
(5)碱石灰增重4.4g,则反应中生成的CO2的质量就是4.4g,物质的量是0.1mol。则根据碳原子守恒可知,碳酸氢铵的物质的量也是0.1mol,质量是7.9g,所以混合物中NH4HCO3的质量分数为 。
。
(6)由于空气中也含有水蒸气和CO2,也能被碱石灰吸收,所以从定量测定的准确性考虑,该套装置还应作进一步的改进是在B之后再接一个阻止空气中水蒸气和二氧化碳进入B的装置。
点评:该题是高考中的常见题型,属于中等难度的试题,试题综合性强,难易适中,在注重对学生基础知识检验与巩固的同时,侧重对学生能力的培养和实验能力的训练与指导。有助于培养学生规范、严谨的实验设计能力,提高学生的综合实验能力,提升学生的学科素养。该类试题重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。
本题难度:一般