时间:2021-02-18 06:59:33
1、填空题 (14分)化学反应原理在科研和工农业生产中有广泛应用。
(1)某化学兴趣小组进行工业合成氨的模拟研究,反应的方程式为N2(g)+3H2(g)  2NH3(g) ΔH<0。在lL密闭容器中加入0.1 mol N2和0.3mol H2,实验①、②、③中c(N2)随时间(t)的变化如下图所示:
2NH3(g) ΔH<0。在lL密闭容器中加入0.1 mol N2和0.3mol H2,实验①、②、③中c(N2)随时间(t)的变化如下图所示: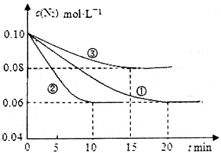
实验②从初始到平衡的过程中,该反应的平均反应速率v(NH3)=__________________;与实验①相比,实验②和实验③所改变的实验条件分别为下列选项中的__________、__________(填字母编号)。
A.增大压强
B.减小压强
C.升高温度
D.降低温度
E.使用催化剂
(2)已知NO2与N2O4可以相互转化:2NO2(g) N2O4(g)。
N2O4(g)。
①T℃时,将0.40 mol NO2气体充入容积为2L的密闭容器中,达到平衡后,测得容器中c(N2O4)="0.05" mol/L,则该反应的平衡常数K=_______________;
②已知N2O4在较高温度下难以稳定存在,易转化为NO2,若升高温度,上述反应的平衡常数K将_____________(填“增大”、“减小”或“不变”)。
③向绝热密闭容器中通入一定量的NO2,某时间段内正反应速率随时问的变化如图所示。下列说法正确的是__________(填字母编号)。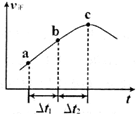
A.反应在c点达到平衡状态
B.反应物浓度:a点小于b点
C.Δt1=Δt2时,NO2的转化率:a~b段小于 b~c段
(3)25℃时,将amol/L的氨水与b mol/L盐酸等体积混合,反应后溶液恰好显中性,则a______b。 (填“>”、“<”或“=”);用a、b表示NH3 H2O的电离平衡常数Kb=________________。
H2O的电离平衡常数Kb=________________。
参考答案:(14分)(1)0.008mol/(L·min)(2分);E(1分);C(1分)
(2)①5L/mol(2分) ②减小(2分),③C(2分);
(3)>(2分) 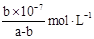 (2分)
(2分)
本题解析:(1)根据图示可知实验②从初始到平衡的过程中,该反应的平均反应速率v(N2)=(0.1mol/L-0.06mol/L)÷10min=0.004mol/(L·min),由于v(NH3):v(N2)=2:1,所以v(NH3)="2" v(N2)=0.008mol /(L·min);与实验①相比,实验②达到平衡所需要的时间短,反应速率快,而物质的平衡浓度没有变化,说明平衡没有发生移动,则所改变的实验条件是加入催化剂,选项是E;而实验③达到平衡所需要的时间短,反应速率快,而物质N2的平衡浓度比①高,说明平衡向逆反应方向移动,所改变的实验条件是升高温度,选项是C;(2)已知NO2与N2O4可以相互转化:2NO2(g)  N2O4(g)。①T℃时,将0.40 mol NO2气体充入容积为2L的密闭容器中,在反应开始时c(NO2)=0.20mol/L.达到平衡后,测得容器中c(N2O4)="0.05" mol/L,根据方程式中物质反应的关系可知,消耗?c(NO2)=0.10mol/L.,所以c(NO2)(ph)=0.10mol/L.则该反应的平衡常数K=
N2O4(g)。①T℃时,将0.40 mol NO2气体充入容积为2L的密闭容器中,在反应开始时c(NO2)=0.20mol/L.达到平衡后,测得容器中c(N2O4)="0.05" mol/L,根据方程式中物质反应的关系可知,消耗?c(NO2)=0.10mol/L.,所以c(NO2)(ph)=0.10mol/L.则该反应的平衡常数K=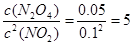 (mol/L);②已知N2O4在较高温度下难以稳定存在,易转化为NO2,说明升高温度,平衡逆向移动,根据平衡移动原理:升高温度,平衡向吸热反应方向移动,正反应是放热反应。则升高温度上述反应的平衡常数K将减小;③A.根据图像可知正反应速率随时间的延长而升高,说明反应正向进行,反应在c点时显示的速率最大,但此时反应可能处于平衡状态,也可能未达到判断,延长不能判断反应是否处于平衡状态,错误;B.由于反应是从正反应方向开始的,所以反应物的浓度会逐渐减小,当达到平衡时达到最小值,所以反应物浓度:a点大于b点,错误;C.由于正反应是放热反应,所以Δt1=Δt2时,温度在b~c段高于a~b段,因为温度对速率的影响大于浓度的影响,所以NO2的转化率:a~b段小于 b~c段,正确。(3)25℃时,将amol/L的氨水与b mol/L盐酸等体积混合,若二者的物质的量相等,则反应恰好产生NH4Cl,该盐是强酸弱碱盐,水解使溶液显酸性,若反应后溶液恰好显中性,则氨水应该稍微过量,所以a>b;NH3·H2O
(mol/L);②已知N2O4在较高温度下难以稳定存在,易转化为NO2,说明升高温度,平衡逆向移动,根据平衡移动原理:升高温度,平衡向吸热反应方向移动,正反应是放热反应。则升高温度上述反应的平衡常数K将减小;③A.根据图像可知正反应速率随时间的延长而升高,说明反应正向进行,反应在c点时显示的速率最大,但此时反应可能处于平衡状态,也可能未达到判断,延长不能判断反应是否处于平衡状态,错误;B.由于反应是从正反应方向开始的,所以反应物的浓度会逐渐减小,当达到平衡时达到最小值,所以反应物浓度:a点大于b点,错误;C.由于正反应是放热反应,所以Δt1=Δt2时,温度在b~c段高于a~b段,因为温度对速率的影响大于浓度的影响,所以NO2的转化率:a~b段小于 b~c段,正确。(3)25℃时,将amol/L的氨水与b mol/L盐酸等体积混合,若二者的物质的量相等,则反应恰好产生NH4Cl,该盐是强酸弱碱盐,水解使溶液显酸性,若反应后溶液恰好显中性,则氨水应该稍微过量,所以a>b;NH3·H2O NH4++OH-;当达到电离平衡时c(NH3·H2O)=(a-b)mol/L,c(OH-)=10-7mol/L,所以NH3
NH4++OH-;当达到电离平衡时c(NH3·H2O)=(a-b)mol/L,c(OH-)=10-7mol/L,所以NH3 H2O的电离平衡常数Kb=
H2O的电离平衡常数Kb=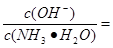
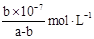 。
。
考点:考查化学反应速率的计算、、化学平衡状态的判断、影响化学平衡的因素、物质的电离平衡产生的表达式的书写的知识。
本题难度:困难
2、选择题 20℃时,H2S的饱和溶液浓度约为0.1mol/L,其电离方程式为:
第一步H2S 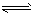 H++HS-;
H++HS-;
第二步HS-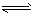 H++S2-。若要使该溶液的c(H+)增大的同时,c(S2-)减小,可采用的措施是
H++S2-。若要使该溶液的c(H+)增大的同时,c(S2-)减小,可采用的措施是
①加入适量的NaOH溶液; ②加入适量的水;③通入适量的SO2;④加入适量硫酸铜固体;
⑤加入少量盐酸
[? ]
A.①③⑤
B.②④⑤
C.②③
D.④⑤
参考答案:D
本题解析:
本题难度:一般
3、选择题 常温下,浓度均为0.1mol/L的三种溶液:①CH3COOH溶液、②NaOH溶液、③CH3COONa溶液.下列说法不正确的是( )
A.溶液的pH:②>③>①
B.水电离出的c(OH-):③>①>②
C.②和③等体积混合后的溶液:c(Na+)+c(H-)=c(OH-)+c(CH3COO-)
D.①和②等体积混合后的溶液:c(CH3COOH)+c(CH3COO)=0.1mol/L
参考答案:D
本题解析:
本题难度:简单
4、选择题 下列事实不能说明一元酸HA是弱酸的是
A.中和一定的NaOH溶液,需消耗与NaOH等物质的量的HA
B.将pH=4的HA溶液稀释10倍,溶液pH小于5
C.将pH=2的HA溶液与pH=12的NaOH溶液等体积混合后,溶液呈酸性
D.将0.1mol/L的HA溶液与0.1 mol/L的NaOH溶液等体积混合后,溶液呈碱性
参考答案:A
本题解析:用实验证明某酸为弱酸,可从下列四个方面进行:(1)利用弱电解质不能全部电离;(2)用电离平衡移动原理,即在外界条件发生时发生移动;(3)综合利用强酸制备弱酸以及电解质不能完全电离;(4)利用盐类水解。
A.酸碱中和滴定的终点为酸碱恰好完全反应,中和滴定的终点不一定为中性;
B.将pH=4的HA溶液稀释10倍,溶液pH小于5,说明酸HA并未完全电离;
C.将pH=2的HA溶液与pH=12的NaOH溶液等体积混合后,溶液呈 酸性。根据规律:酸碱等体积混合pH相加得14,谁弱谁过量,谁弱显谁性,溶液显酸性,酸为弱酸;
D.一元酸碱等体积等浓度混合,恰好完全反应,生成盐,溶液显碱性,说明为强碱弱酸盐,酸为弱酸。
本题难度:一般
5、填空题 (10分)
Ⅰ、A物质的化学式为M(OH)2,将其溶于水制成稀溶液,该溶液呈中性,在溶液中存在:
M2+ + 2OH-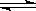 ?M(OH)2
?M(OH)2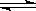 ?2H+ + MO22-
?2H+ + MO22-
回答以下题目一律用“增大”“减小”“不变”填空
(1)在其他条件不变的情况下,25Co时,在蒸馏水中加入A物质后,与加入前比较,
①由水电离出的C(OH-)?,C(H+)?,水的电离度?,Kw?
(2)(4分)25Co时,向A的稀溶液中加入少量的烧碱固体。
则水的电离度?,溶液的pH?
Ⅱ、.(2分)室温下,甲、乙两瓶氨水的浓度分别为1mol/L和0.1mol/L,则甲、乙两瓶氨水中C(OH-)之比为??10 (填大于、等于或小于)
参考答案:(10分)
Ⅰ、(1)
①C(OH-)变大?,C(H+)变大变,水的电离度变小?,Kw?不变?
(2)
则水的电离度?不变?,溶液的pH不变?
Ⅱ、.(2分)C(OH-)之比为?等于??10 (填大于、等于或小于)
本题解析:略
本题难度:一般