时间:2021-02-18 05:54:16
1、填空题 (1)下列盐溶液中能发生水解的用离子方程式表示,不能发生水解的请写上“不发生水解”字样,并说明溶液的酸碱性:
K2CO3______,溶液呈______性;
K2SO4______,溶液呈______性;
NH4Cl______,溶液呈______性.
(2)物质的量浓度均为0.1mol/L的下列溶液:①KNO3、②Na2CO3、③NaHCO3、④NaHSO4、⑤CH3COOH、⑥NaOH、⑦Ba(OH)2、⑧NH4Cl,pH由大到小的顺序为:______(填数字代号)
(3)现有常温下的0.1mol?L-1Na2CO3溶液:
①你认为该溶液呈碱性的原因是(用离子方程式表示)______;
②为证明你的上述观点,请设计一个简单的实验,简述实验过程______.
参考答案:(1)K2CO3是强碱弱酸盐,水解后水溶液都呈碱性,水解离子方程式为CO32-+H2O?HCO3-+OH-,
Na2SO4是强酸强碱盐,不水解,溶液呈中性;
NH4Cl是强酸弱碱盐,水解后溶液呈酸性,水解离子方程式为NH4++H2O?NH3?H2O+H+,
故答案为:CO32-+H2O?HCO3-+OH-;碱;不水解;中性;NH4++H2O?NH3?H2O+H+;酸;
(2)酸:⑤CH3COOH是弱电解质,所以只有部分电离,故c(H+)<0.1mol/L,所以pH>1;
碱:⑥NaOH是强电解质,完全电离,c(OH-)=0.1mol/L,所以pH=13;
⑦Ba(OH)2是强电解质,完全电离,c(OH-)=0.2mol/L,所以pH=13.7;
盐:④NaHSO4是强酸酸式盐,在水中完全电离成钠离子、硫酸根离子、氢离子,所以c(H+)=0.1mol/L,所以pH=1;
⑧NH4Cl是强酸弱碱盐,水解后溶液呈酸性,1<pH值<7;
①KNO3是强酸强碱盐,水溶液呈中性,pH=7;
②Na2CO3是强碱弱酸盐,水溶液都呈碱性;
③NaHCO3是弱酸的酸式盐水解显碱性,水解程度小于Na2CO3 ,碱性小于Na2CO3,所以pH由大到小的顺序为:⑦>⑥>②>③>①>⑧>⑤>④,
故答案为:⑦>⑥>②>③>①>⑧>⑤>④;
(3)①Na2CO3是强碱弱酸盐,水解后水溶液都呈碱性,其水解离子方程式为:CO32-+H2O?HCO3-+OH-,
故答案为;CO32-+H2O?HCO3-+OH-;
②向Na2CO3溶液中加酚酞试液,溶液变红色,说明溶液显碱性,证明Na2CO3水解,
故答案为:向Na2CO3溶液中加酚酞试液,溶液变红色,说明溶液显碱性,证明Na2CO3水解.
本题解析:
本题难度:一般
2、填空题 (6分)写出下列盐水解的离子方程式:
① CH3COONa
② (NH4)2SO4
③ NaHCO3
参考答案:(6分)(1)①CH3COO-+H2O CH3COOH+OH- ②NH4++H2O
CH3COOH+OH- ②NH4++H2O NH3·H2O+H+
NH3·H2O+H+
③HCO3-+H2O H2CO3+OH-(以上每空2分)
H2CO3+OH-(以上每空2分)
本题解析:略
本题难度:一般
3、填空题 (16分)I.合成氨的原料气H2可通过反应CO(g)+H2O(g)  CO2 (g) +H2(g) 获取。
CO2 (g) +H2(g) 获取。
(1)T ℃时,向容积固定为5 L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO的浓度为0.08 mol·L-1,则平衡时CO的转化率为 ,该温度下反应的平衡常数K值为 。
(2)保持温度仍为T ℃,改变水蒸气和CO的初始物质的量之比,充入固定容器中进行反应,下列描述能够说明体系处于平衡状态的是 (填序号)。
a.容器内压强不随时间改变
b.混合气体的密度不随时间改变
c.单位时间内生成a mol CO2的同时消耗a mol H2
d.混合气中n (CO) : n (H2O) : n (CO2) : n (H2) = 1 : 16 : 6 : 6
II.(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨在燃烧实验中相关的反应有:
①4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H1
②4NH3(g)+5O2(g)=4NO(g)+6H2O(l) △H2
③4NH3(g)+6NO(g)=5N2(g)+6H2O(l) △H3
请写出上述三个反应中△H1、△H2、△H3三者之间关系的表达式,△H1= 。
(2)美国Simons等科学家发明了使NH3直接用于燃料电池的方法,其装置用铂作为电极、加入碱性电解质溶液,其电池反应为4NH3+3O2=2N2+6H2O
①写出该燃料电池的正极反应式 。
②若用该燃料电池产生的电能在铁皮上镀锌(制白铁皮),某铁皮上现需要镀上9.75g锌,理论上至少需要消耗标准状况的氨气 L。
III.(1)下图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。由图可知Mg与卤素单质的反应均为 (填“放热”或“吸热”)反应。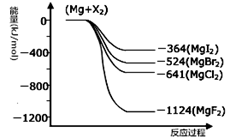
(2)金属Mg与CH3Cl在一定条件下反应可生成CH3MgCl,CH3MgCl是一种重要的有机合成试剂,易与水发生水解反应并有无色无味气体和沉淀生成。写出CH3MgCl水解的化学方程式 。
参考答案:(16分)
I.(1) 60 %(2分) 2.25(2分)
(2) c、d(2分)
II.(1)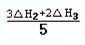 (2分)
(2分)
(2)①O2 + 4e-+ 2H2O  4OH- (2分) ② 2.24 (2分)
4OH- (2分) ② 2.24 (2分)
III.(1)放热 (2分)
(2)2CH3MgCl+H2O=2CH4↑+Mg(OH)2↓+MgCl2或CH3MgCl+H2O=CH4↑+Mg(OH)Cl↓(2分)
本题解析:I.(1)设平衡时CO的浓度减少xmol/L,则
CO(g)+H2O(g)  CO2 (g) +H2(g)
CO2 (g) +H2(g)
开始(mol/L)1/5=0.2 1/5=0.2
转化(mol/L)x x x x
平衡(mol/L)0.2-x 0.2-x x x
根据题意,CO的浓度为0.08 mol·L-1,则0.2-x=0.08,x=0.12,所以CO的转化率是0.12/0.2×100%=60%;
平衡常数K= c(CO2)·c(H2)/c(CO)·c(H2O)=x2/(0.2-x)2=2.25;
(2)a.因为该反应是气体的物质的量不变的可逆反应,则容器内压强始终不随时间改变,不能判断平衡状态,错误;b.因为容器的体积不变,则混合气体的密度始终不随时间改变,不能判断平衡状态,错误; c.单位时间内生成a mol CO2的同时消耗a mol H2,符合正逆反应速率相等,是平衡状态,正确;d.混合气中n (CO) : n (H2O) : n (CO2) : n (H2) = 1 : 16 : 6 : 6时,Qc= c(CO2)·c(H2)/c(CO)·c(H2O)= 6×6/1×16=2.25=K,所以是平衡状态,答案选cd;
II.(1)①中无NO气体,根据盖斯定律,将②×3+③×2 消去NO可得5×①,所以①中的△H1=(3△H2+2△H3)/5;
(2)①根据4NH3+3O2=2N2+6H2O,可知正极是氧气发生还原反应,生成氢氧根离子,所以正极的电极反应式为O2 + 4e-+ 2H2O  4OH-;
4OH-;
②9.75gZn的物质的量是9.75g/65g/mol=0.15mol,则失去电子的物质的量是0.15mol×2=0.30mol,根据得失电子守恒,则氧气得到电子的物质的量是0.30mol,则需要氧气的体积是0.30mol/4×22.4L/mol=1.68L,所以氨气的体积是1.68L×4/3=2.24L.
III.(1)由图可知,反应物的总能量大于生成物的总能量,所以反应为放热反应;
(2)CH3MgCl易与水发生水解反应并有无色无味气体和沉淀生成,该沉淀为氢氧化镁沉淀,根据元素守恒,则该气体中含C元素,为甲烷气体,同时还有氯化镁生成,则反应的化学方程式为2CH3MgCl+H2O=2CH4↑+Mg(OH)2↓+MgCl2。
考点:考查化学平衡的判断、计算,电化学反应原理的应用,化学方程式的判断与书写
本题难度:困难
4、填空题 回答下列问题:
(1)有一种溶液除H+、OH-外,还有Na+、SO42-和Cl-,测得三种离子的浓度分别是0.01 mol·L-1、0.0035 mol·L-1和 0.004 mol·L-1,该溶液的pH为______________ 。
(2) NH4Cl溶液显酸性,试用离子方程式表示这一反应_________________ 。
(3)液氨类似于水的电离,试写出液氨的电离方程式___________________;在液氨中加入NH4Cl,则平衡将向__________移动。
(4)pH相同的氨水和氢氧化钠溶液,分别用蒸馏水稀释至原来体积的m倍和n倍,稀释后两溶液的pH仍相同,则m____n(选填“>”“<”或“=”);若改用pH相同的盐酸和硫酸溶液,进行上述操作,则m________n(选填“>” “<”或“=”)。
参考答案:(1)3
(2) H2O+ NH4+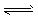 NH3·H2O+H+
NH3·H2O+H+
(3)2NH3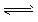 NH4++ NH2- ;逆反应方向
NH4++ NH2- ;逆反应方向
(4) >; =
本题解析:
本题难度:一般
5、选择题 为了使K2S溶液中c(K+)/c(S2-)的比值变小,可加入的物质是
①适量HCl(g);②适量NaOH(s);③适量KOH(s);④适量NaHS(s);⑤适量的水
A.②④
B.①②⑤
C.③④⑤
D.②③
参考答案:A
本题解析:S2-+H2O=OH-+HS-,S2—的水解平衡逆向移动,[K+]/[S2—]的比值变小。①氢离子浓度增大,使水解平衡正向移动,错误;②氢氧根离子浓度增大,使水解平衡逆向移动,正确;③②氢氧根离子浓度增大,使水解平衡逆向移动,但K+浓度增大,错误;④HS-浓度增大,使水解平衡逆向移动,正确;⑤加水稀释,各离子浓度都减小,平衡正向移动,S2-数目减少,[K+]/[S2—]的比值增大。
考点:考查化学平衡移动。
本题难度:一般