时间:2021-02-18 04:45:31
1、选择题
下列物质中,含有非极性共价键的离子化合物的是 (? )
A.NH4NO3
B.Cl2
C.H2O2
D.Na2O2
2、填空题 如图所示的结构为高温超导领域里的一种化合物―钙钛矿晶体结构,该结构是其晶体中具有代表性的最小重复单位。 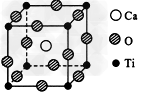
?(1)在该物质的晶体结构中,每个钛离子周围与它 ?最接近且距离相等的钛离子、钙离子各有_____个、?______个。 ?
(2)该晶体结构中,氧、钛、钙的原子个数比是____,该物质的化学式可表示为____。
(3)若钙、钛、氧三元素的相对原子质量分别为a、b、c,晶体结构图中正方体边长(钛原子之间的距离)为d?nm(1?nm=?10-9?m),则该晶体的密度为________g/cm3。
3、选择题 如图所示的是某原子晶体A空间结构的一个单元,A与某物质B反应生成C,其实质是每个A-A键中插入一个B原子,则C物质的化学式为( ? )
A.AB
B.AB4
C.AB2
D.A2B5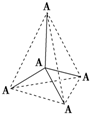
4、填空题 已知晶胞中微粒数的计算方法―切割法,我们可以用“切割法”来计算一 ?个晶胞中实际拥有的微粒数。切割法的根本原则是:晶胞任意位置的一个原子如被x个晶胞所共有,那么,每个晶胞对这个原子分得的份额就是______________。
5、选择题 金属晶体的下列性质中,不能用金属晶体结构加以解释的是
A.易导电
B.易导热
C.有延展性
D.易锈蚀