时间:2021-02-18 04:40:47
1、选择题 将物质的量均为a?mol的钠和铝一同投入m?g水中(水足量),所得溶液的密度为ρg?Cm-3,则此溶液的物质的量浓度为
A.mol/L
B.mol/L
C.mol/L
D.mol/L
参考答案:C
本题解析:分析:将物质的量均为a?mol的钠和铝投入足量水中发生反应:2Na+2H2O=2NaOH+H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,由方程式可知,溶液为偏铝酸钠溶液,偏铝酸钠的物质的量为amol.根据方程式计算生成氢气的物质的量,在计算氢气质量,溶液质量为m(溶液)=m(金属)+m(H2O)-m(H2),据此计算溶液质量,利用V=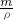 计算溶液体积,再利用c=
计算溶液体积,再利用c=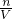 计算溶液物质的量浓度.
计算溶液物质的量浓度.
解答:钠和铝投入足量水中发生反应:2Na+2H2O=2NaOH+H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
由方程式可知,a?mol的钠反应生成amol氢氧化钠,生成氢气0.5amol;amol氢氧化钠与amol铝恰好反应生成amol偏铝酸钠,同时生成氢气1.5amol.溶液为偏铝酸钠溶液.
所以氢气的质量为(0.5amol+1.5amol)×2g/mol=4ag;
所以溶液质量m(溶液)=m(金属)+m(H2O)-m(H2)=amol×23g/mol+amol×27g/mol+mg-4ag=(46a+m)g,
所以溶液的体积为 =
=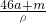 ml
ml
所以溶液的物质的量浓度为 =
=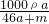 mol/L.
mol/L.
故选:C.
点评:考查物质的量浓度的计算,难度中等,判断溶液是偏铝酸钠是解题关键,然后利用物质的量浓度定义式计算.理解物质的量浓度的概念.
本题难度:一般
2、选择题 设NA表示阿伏加德罗常数的值,下列说法正确的是(? )
A.5.6 g铁粉在0.1 mol氯气中充分燃烧,转移电子数为0.3NA
B.1 mol Na2O2与足量H2O充分反应,转移的电子数为2NA
C.7.8 g Na2O2中含有的阴离子数等于0.1NA
D.0.5 mol雄黄(As4S4,结构如下图)中含有NA个S―S键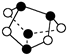
参考答案:C
本题解析:5.6 g铁粉与0.1 mol氯气反应,铁粉过量,转移电子数为0.2NA,A项错误;Na2O2与水的反应为自身氧化还原反应,1 mol Na2O2与足量水反应转移电子数为NA,B项错误;Na2O2的阴离子为O22-,故7.8 g Na2O2所含的阴离子数为0.1NA,C项正确;从成键角度分析,黑球、白球分别为砷、硫,故0.5 mol雄黄中含NA个As―As键,不含S―S键,D项错误。
本题难度:一般
3、选择题 下列说法正确的是
A.17 g NH3中含有6.02×1023个电子
B.65 g Zn与足量稀盐酸反应转移1 mol e-
C.100 mL 1 mol/L NaOH溶液中含有1 mol OH-
D.标准状况下,11.2 L O2中约含有6.02×1023个氧原子
参考答案:D
本题解析:氨气是10电子微粒,17g氨气是1mol,含有10mol电子,A不正确;锌再反应中失去2个电子,65g锌是1mol,失去2mol电子,B不正确;100 mL 1 mol/L NaOH溶液中含有0.1 mol OH-,C不正确,所以答案选D。
点评:阿伏加德罗常数是历年高考的“热点”问题。多年来全国高考化学试题重现率几乎为100%。考查阿伏加德罗常数的应用的题目,为高考必考题目,这是由于它既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,又可以涵盖多角度的化学知识内容。要准确解答好这类题目,一是要掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系;二是要准确弄清分子、原子、原子核内质子中子及核外电子的构成关系。其解题的方法思路是,在正确理解有关概念的基础上,将各物质的质量、气体的体积、溶液的浓度等转化为指定粒子的物质的量(mol)进行判断。
本题难度:一般
4、选择题 碳酸铜和碱式碳酸铜均可溶于盐酸,转化为氯化铜。在高温下这两种化合物均能分解成氧化铜。溶解28.4g上述混合物,恰好消耗1mol/L盐酸500mL。灼烧等质量的上述混合物,得到氧化铜的质量是(?)
A.35g
B.30 g
C.20 g
D.15 g
参考答案:C
本题解析:有关的化学反应方程式为: CuCO3+2HCl=CuCl2+ CO2↑+H2O. Cu2 (OH)2CO3+4HCl=2CuCl2+ CO2↑+2H2O. CuCO3 CuO+ CO2↑;Cu2 (OH)2CO3
CuO+ CO2↑;Cu2 (OH)2CO3 2CuO+ CO2↑+H2O.溶解固体时最后得到的是CuCl2。n(Cu)="1/2n(HCl)=1/2×1mol/L×0.5L=0.25mol." 若是灼烧等质量的上述混合物,得到氧化铜的物质的量与上述的相同。n(CuO)="n(Cu)=" 0.25mol.所以m(CuO)= n(CuO)・M=0.25mol×80g/mol=20g.所以正确选项为:C。
2CuO+ CO2↑+H2O.溶解固体时最后得到的是CuCl2。n(Cu)="1/2n(HCl)=1/2×1mol/L×0.5L=0.25mol." 若是灼烧等质量的上述混合物,得到氧化铜的物质的量与上述的相同。n(CuO)="n(Cu)=" 0.25mol.所以m(CuO)= n(CuO)・M=0.25mol×80g/mol=20g.所以正确选项为:C。
本题难度:一般
5、选择题 由硫酸钾、硫酸铝和硫酸组成的混合溶液,其pH=1,c(Al3+)=0.4mol・L-1,c(SO42-)=0.8mol・L-1;则
c(K+)为
[? ]
参考答案:C
本题解析:
本题难度:简单