时间:2021-02-18 04:39:24
1、选择题 苯是一种不溶于水的无色液体,有特殊气味,密度比水小,沸点为80.1 ℃。现有苯和水的混合物,能将苯从该混合物中提取出来的最合理的方法是(? )
A.过滤
B.分液
C.萃取
D.蒸馏
参考答案:B
本题解析:由于苯和水互不相溶,所以可以采用分液法将苯分离出来。
本题难度:简单
2、选择题 下列实验设计和结论相符合的是?
A.将碘水倒入分液漏斗,加入适量乙醇,振荡后静置,可将碘萃取到乙醇中
B.某气体能使湿润的红色石蕊试纸变蓝,该气体一定显碱性
C.在蒸馏水中加入少量FeCl3固体,可得纯净的FeCl3溶液
D.某无色溶液中加入Ba(NO3)2溶液,再加稀盐酸,沉淀不溶解,则原溶液中一定有SO42-
参考答案:B
本题解析:
正确答案:B
A、乙醇与水互溶,不分层;B、正确;C、不正确,FeCl3水解;D、不正确,可能是SO32―
本题难度:一般
3、简答题 某活动课程小组拟用50mLNaOH溶液吸收CO2气体,制备Na2CO3溶液.为了防止通入的CO2气体过量生成NaHCO3,设计了如下实验步骤:
a.取25mL?NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;
b.小火煮沸溶液1~2min;
c.在得到的溶液中加入另一半(25mL)NaOH溶液,使其充分混合反应.
(1)此方案能制得较纯净的Na2CO3,写出a、c两步的化学反应方程式______、______.
此方案第一步的实验装置如图所示: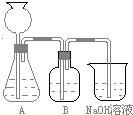
(2)加入反应物前,如何检查整个装置的气密性?______(3)装置B中盛放的试剂是______,作用是______.
(4)在实验室通常制法中,装置A还可作为下列______气体的发生装置(填序号).
①CH2═CH2?②H2S?③CH4?④CH≡CH?⑤H2
(5)实验室制取下列气体:①NH3,②Cl2,③HCl,④H2S,⑤CH4,⑥CO,⑦CO2,⑧O2时,属于必须进行尾气处理,并能用下图所示装置进行处理的,将气体的序号填入装置图的下方空格内.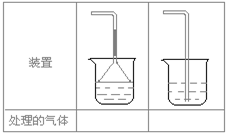
(6)已知所用NaOH溶液中溶质的质量分数为40%,室温下该溶?液密度为1.44g/mL,假设反应前后溶液的体积不变,不考虑实验误差,计算用此种方法制备所得Na2CO3溶液的物质的量浓度为______.
参考答案:(1)因过量的CO2与NaOH溶液反应生成NaHCO3,其反应为NaOH+CO2═NaHCO3,因酸式盐与碱反应生成盐和水,其反应为NaHCO3+NaOH═Na2CO3+H2O,
故答案为:NaOH+CO2═NaHCO3;NaHCO3+NaOH═Na2CO3+H2O;?
(2)因装置不漏气时,通过改变气体的体积可以改变压强,故答案:用弹簧夹夹住A、B连接处,先检查A的气性:塞紧橡皮塞,从漏斗注入一定量的水,使漏斗中的水面高于锥形瓶内的水面,停止加水后,漏斗内与锥形瓶中的液面差保持不变,说明装置不漏气.然后检查B的气密性:向烧杯中注入少量水,使导管口侵入水中,双手捂住广口瓶片刻有气泡冒出,松开手后,有少量水进入导管形成水柱,说明装置不漏气(也可一次检查A、B的气密性:连接和烧杯间的乳胶管用止水夹夹住.然后从漏斗注入一定量的水,使漏斗中的水面高于锥形瓶内的水面,过一会,观察漏斗内与锥形瓶中的液面差,若保持不变,说明装置不漏气);
(3)因CO2中含有HCl,要得到纯净的CO2,必须除去HCl,同时除杂试剂不能CO2反应,所以用饱和NaHCO3溶液而不能用饱和Na2CO3溶液,故答案:饱和酸氢钠溶液;吸收HCl气体;
(4)因制备CO2、H2S、CH≡CH、H2装置的特点:固体+液体→气体,而制备CH2═CH2?装置的特点:液体+液体加热
本题解析:
本题难度:一般
4、实验题 (14分)实验室配制480 mL 0.5mol/L的NaOH溶液,请填写下列空白:
(1)本实验所必需的仪器有:天平、药匙、烧杯、玻璃棒、________________、_______________。
(2)配制该溶液需取NaOH晶体________________g。
(3)某同学俯视观察液面,会使所配溶液浓度__________(填“偏高”、“偏低”或“无影响”,下同)。
某同学溶解后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会__________
某同学称量氢氧化钠固体时称量时间过长,所配溶液浓度会__________
(4)若实验过程中出现如下情况应如何处理?加蒸馏水时不慎超过了刻度,应_____________________。
参考答案:
本题解析:略
本题难度:一般
5、实验题 (13分)
Ⅰ.下图所示是分离混合物时常用的仪器,回答下列问题: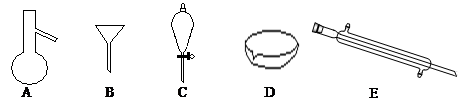
(1)写出仪器A、C、E的名称?
(2)分离以下混合物应该主要选用什么仪器?(填字母符号)食用油和酒精:??汽油和水:?
Ⅱ.实验室用固体烧碱配制200 mL? 0.5 mol·L-1的NaOH溶液。
(1)需称量_________ g 烧碱,应放在___________中称量、溶解。
(2)完成此配制实验,除了量筒,烧杯,玻璃棒外还需要的常见的玻璃仪器有___________
(3)请描述定容操作应采取的具体方法_____________________________。
参考答案:Ⅰ(1)蒸馏烧瓶、分液漏斗、冷凝器?(2)A E、C
Ⅱ(1)5.0(2分);?100 mL烧杯?(2)250 mL容量瓶,胶头滴管?
(3)向容量瓶中注入蒸馏水至刻度线下1~2 cm处,改用胶头滴管滴加蒸馏水至溶液的?凹液面正好与刻度线相切
本题解析:I.A仪器叫蒸馏烧瓶,用于蒸馏实验;B仪器叫漏斗,用于过滤实验;C仪器叫分液漏斗,用于萃取分液实验;D仪器叫蒸发皿,用于蒸发实验;E仪器叫冷凝管,用于蒸馏实验。食用油和酒精互溶的两种液体,用蒸馏的方法分离,汽油和水互不相溶的两种液体用分液的方法分离。
II.配制200 mL? 0.5 mol·L-1的NaOH溶液,由于没有200mL容量瓶,所以需要用250mL容量瓶,因此需要NaOH0.125mol,应称量5.0g,NaOH固体属于易潮解物质,因此要放在烧杯或者表面皿上称量。配制实验除了量筒,烧杯,玻璃棒外还需要的常见的玻璃仪器有250 mL容量瓶和胶头滴管,定容操作具体方法:向容量瓶中注入蒸馏水至刻度线下1~2 cm处,改用胶头滴管滴加蒸馏水至溶液的?凹液面正好与刻度线相切。
点评:本题以考实验基础为主,比较简单。
本题难度:一般