时间:2020-08-23 08:18:45
1、选择题 室温下,pH相同体积相同的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是
[? ]
A. 加水稀释2倍后,两溶液的pH均减小
B. 使温度都升高20℃后,两溶液的pH均不变
C. 加适量的醋酸钠晶体后,两溶液的pH均增大
D. 加足量的锌充分反应后,醋酸产生的氢气比盐酸少
参考答案:C
本题解析:
本题难度:一般
2、填空题 硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离。但事实是,硫酸在水中的第一步电离是完全的,第二步电离并不完全,其电离情况为:H2SO4=H++HSO4-,HSO4- H++SO42-.
H++SO42-.
请据此回答下列有关问题:
(1)Na2SO4溶液呈?(填“弱酸性”、“中性”或“弱碱性”),原因是:?(用离子方程式表示)
(2)写出H2SO4溶液与BaCl2溶液反应的离子方程式:?;
(3)在0.1 mol・L-1的Na2SO4溶液中,下列粒子浓度关系式正确的是?。(填编号)?
A.c(SO42-)+c(HSO4-)=0.1 mol・L-1
B.c(SO42-)+c(HSO4-)=2 c(Na+)
C.c(OH-)=c(H+)+c(HSO4-)
D.c(Na+)+c(H+)=c(OH-)+c(HSO4-)
(4)已知0.1 mol・L-1的NaHSO4溶液的pH=2,则0.1 mol・L-1的H2SO4溶液中SO42-的浓度?0.01mol・L-1(填“>” “="”" 或“<”)。
参考答案:(1)弱碱性 ;SO42-+H2O  ?HSO4―+ OH―(2)HSO4-+Ba2+ = BaSO4↓+ H+?
?HSO4―+ OH―(2)HSO4-+Ba2+ = BaSO4↓+ H+?
(3)AC?(4)<
本题解析:硫酸的第一步电离是完全的:H2SO4=H++HSO4-,第二步电离并不完全:HSO4- H++SO42-.(1)根据题给信息Na2SO4溶液存在SO42-的水解平衡:SO42-+H2O
H++SO42-.(1)根据题给信息Na2SO4溶液存在SO42-的水解平衡:SO42-+H2O OH-+HSO4-,溶液呈弱碱性;
OH-+HSO4-,溶液呈弱碱性;
(2)硫酸溶液中存在HSO4-离子,难电离,硫酸与氯化钡溶液反应的离子方程式为:HSO4-+Ba2+=BaSO4↓+H+,
(3)0.lmol?L-1Na2SO4溶液中离子浓度关系:根据物料守恒,c(?Na+)=2c(SO42-)+2c(HSO4-)=0.2mol?L-1,A项正确,B项错误;根据质子守恒:c(OH-)=c(?HSO4-)+c(H+),C项正确;根据电荷守恒:c(?Na+)+c(H+)=c(OH-)+c(HSO4-)+2c(SO42-),C项错误;选AC;
(4)0.1 mol・L-1NaHSO4溶液的pH=2,根据电离方程式判断c(SO42-)=0.01mol?L-1,而0.1mol?L-1H2SO4溶液中氢离子浓度比硫酸氢钠溶液中大,对硫酸氢根离子的电离起抑制作用,所以c(?SO42-)<0.01mol?L-1。
本题难度:一般
3、填空题 对于弱酸,在一定温度下达到电离平衡时,各粒子的浓度存在一种定量的关系.若25℃时有HA? H++A-,则K=
H++A-,则K=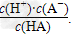 式中:K为电离平衡常数,只与温度有关,c为各粒子的平衡浓度.下表是几种常见弱酸的电离平衡常数(25℃).
式中:K为电离平衡常数,只与温度有关,c为各粒子的平衡浓度.下表是几种常见弱酸的电离平衡常数(25℃). 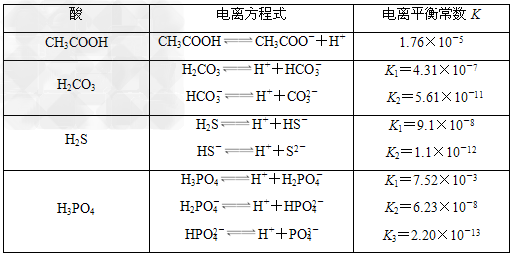
回答下列各题:
(1)K只与温度有关,当温度升高时,K值________(填“增大”、“减小”或“不变”).
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关系?________.
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、H2PO4-、HPO42-都看作是酸,其中酸性最强的是________,最弱的是________.
(4)多元弱酸是分步电离的,每一步都有相应的电离平衡常数,对于同一种多元弱酸的K1、K2、K3之间存在着数量上的规律,此规律是________,产生此规律的原因是________________________________________.
参考答案:(1)增大
(2)K值越大,电离出的氢离子浓度越大,所以酸性越强
(3)H3PO4 ;HPO42-
(4)K1∶K2∶K3≈1∶10-5∶10-10 ;上一级电离产生的H+对下一级电离有抑制作用
本题解析:
本题难度:一般
4、选择题 下列关于室温下氨水的叙述,正确的是
[? ]
A. 相同浓度的氨水和NaOH溶液,能分别与相同浓度的盐酸恰好中和
B. 加水稀释0.10 mol/L的氨水,溶液中n(OH-)减小
C. 若温度不变,在氨水中加入少量NH4Cl固体,NH3・H2O的电离平衡常数变小
D. 氨水中的离子浓度关系满足:c(OH-)=c(H+)+c(NH4+)
参考答案:D
本题解析:
本题难度:一般
5、选择题 化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是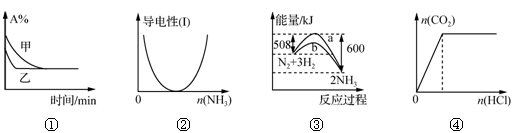
A.图①表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
B.图②表示CH3COOH溶液中通入NH3至过量的过程中溶液导电性的变化
C.图③表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂
D.图④表示一定浓度Na2CO3溶液中滴加盐酸,生成CO2与滴加盐酸物质的量的关系
参考答案:C
本题解析:A、该反应为体积缩小的反应,增大压强,平衡正移,但甲乙两曲线平衡状态相同,故该图不应是压强的影响,而应是催化剂的影响,错误;B、乙酸为弱电解质,其中通入氨气后导电能力逐渐增强,错误;C、由图可知,反应物的总能量大于生成物的总能量,为放热反应,b曲线表示反应的活化能降低,说明加入了催化剂,正确;D、碳酸钠溶液中加入盐酸,刚开始不会生成二氧化碳气体,错误;故本题选择C。
考点:化学图像的描述
本题难度:困难