时间:2020-08-23 08:02:45
1、选择题 锂电池是一代新型高能电池,它以质量轻、能量高而受到了普遍重视,目前已研制成功多种锂电池。某种锂电池的总反应式是Li+MnO2=LiMnO2。下列说法正确的是
[? ]
A.Li是负极,电极反应为Li-e-=Li+
B.Li是正极,电极反应为Li+e-=Li-
C.MnO2是负极,电极反应为MnO2+e-=MnO2-
D.锂电池是一种环保型电池
参考答案:AD
本题解析:
本题难度:一般
2、选择题 镁-H2O2酸性燃料电池采用海水作电解质,下列结论错误的是( )
A.正极发生的电极反应为:H2O2+2H++2e-=2H2O
B.电池总反应为:Mg+H2O2=Mg(OH)2
C.工作时,正极周围海水的pH增大
D.电池工作时,溶液中的H+向正极移动
参考答案:A、H2O2具有氧化性,应为原电池的正极,被还原,电极反应式为H2O2+2H++2e-=2H2O,故A正确;
B、电解质溶液呈酸性,不可能生成Mg(OH)2,电池总反应应为H2O2+2H++Mg═Mg2++2H2O,故B错误;
C、工作时,正极反应式为H2O2+2H++2e-═2H2O,不断消耗H+离子,正极周围海水的pH增大,故C正确;
D、原电池中,阳离子向正极移动,阴离子向负极移动,形成闭合回路,故D正确.
故选B.
本题解析:
本题难度:一般
3、选择题 银锌蓄电池是一种高能电池,它的两极材料分别为锌和氧化银,电解质溶液为KOH溶液,该电池反应的化学方程式为:Zn+Ag2O+H2O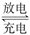 Zn(OH)2+2Ag,下列判断正确的是
Zn(OH)2+2Ag,下列判断正确的是
A.电池放电时,正极区溶液pH减小
B.电池放电完后,需补充注入水
C.负极电极反应式:2Ag+2OH--2e-=Ag2O+H2O
D.正极电极反应式:Ag2O+H2O+2e-=2Ag+2OH-
参考答案:D
本题解析:
正确答案:D
A、不正确,正极电极反应式:Ag2O+H2O+2e-=2Ag+2OH-,产生OH―,pH增大;
B、不正确,充电后又生成水;
C、不正确,负极Zn+2OH― ―2e―=Zn(OH)2
D、正确。
本题难度:一般
4、选择题 电子表所用的某种纽扣电池的电极材料为Zn和Ag2O,电解质溶液是KOH溶液。电池总反应式为:Zn+Ag2O="ZnO+2Ag," 下列说法错误的是 ( )
A.该电池的正极是Ag2O,负极是Zn
B.该电池负极的电极反应式为:Zn+2OH——2e—=ZnO+H2O
C.理论上该电池工作一段时间后,溶液中KOH的浓度不变
D.该电池工作时,电解质中的阴离子向正极移动
参考答案:D
本题解析:略
本题难度:一般
5、选择题 如图是一种正在投入生产的大型蓄电系统的原理图.电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电的化学反应方程式为:2Na2S2+NaBr3
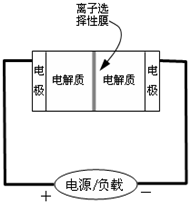
参考答案:①、有0.1molNa+通过离子交换膜,说明有0.1mol电子转移,故①正确;
②、电池放电时,正极反应为得到电子发生的还原反应,正极反应为:NaBr3+2Na++2e-=3NaBr,负极反应氧化反应,负极电极反应式为2Na2S2-2e-=2Na++Na2S4,故②错误;
③、充电过程为电解池,阳离子向阴极移动,由图可知,右侧电极为阴极,充电过程中钠离子从左到右通过离子交换膜,故③错误;
④、放电过程为原电池,阳离子向正极移动,由图可知,左侧电极为正极,放电过程中钠离子从右到左通过离子交换膜,故④正确;
故选D.
本题解析:
本题难度:一般