时间:2020-08-23 07:46:59
1、推断题 下列物质(均为中学化学常见物质)转化关系如图所示,已知D为红棕色粉末(反应条件及部分反应物、产物未全部标出)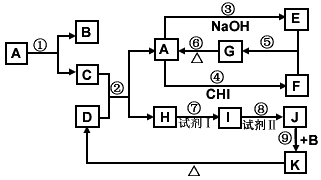
根据图示转化关系填写下列空白:
(1)写出下列物质的化学式:A:________;B:________;E:________;K:________;
(2)C与D的混合物通常叫做________(填名称)。
(3)写出下列化学反应方程式(注明反应条件,若是离子反应的写离子方程式):
①________________;②________________;③________________;
参考答案:(1)A.Al2O3;B.O2;E.NaAlO2;K.Fe(OH)3
(2)铝热剂
(3)①2Al2O3 4Al+3O2↑;②2Al+Fe2O3
4Al+3O2↑;②2Al+Fe2O3 Al2O3+2Fe;③Al3++3AlO2-+6H2O=4Al(OH)3↓
Al2O3+2Fe;③Al3++3AlO2-+6H2O=4Al(OH)3↓
本题解析:
本题难度:一般
2、填空题 A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件及部分产物均未列出)。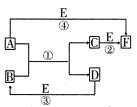
(1)若A、D、E是短周期的非金属单质,且 A、D所含元素同主族,A、E含元素同周期,已知D单质在电子工业中有重要作用,则D的原子结构示意图为________;F的分子构型为________;反应①的化学方程式为__________________。
(2)若A、D为常见金属单质,且加热时A、D才能溶解在E的浓溶液中,写出反应③的化学方程式_ _________________;足量的A与B溶液充分反应后,生成物C中金属阳离子的检验方法为__________________;若以惰性电极电解B的水溶液,当阴极增重9.6g时,阳极生成气体在标准状况下的体积为________,写出电解B的水溶液的离子方程式__________________。
参考答案:
(1)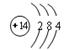 ?直线型? 2C+SiO2
?直线型? 2C+SiO2 2CO↑+Si
2CO↑+Si
(2)Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
取少量C溶液于试管中,滴加KSCN溶液无明显颜色变化,再滴加氯水呈血红色? 1.68 L
2Cu2+ + 2H2O 2Cu + O2↑ + 4H+
2Cu + O2↑ + 4H+
本题解析:(1)A、、E是短周期的非金属单质D在电子工业中有重要作用,则D为Si元素;由于 A、D所含元素同主族,所以A为C元素;能与C单质发生制取Si单质,则B为SiO2;反应的方程式为:C+ SiO2 Si+2CO↑.C为CO气体;2CO+ O2
Si+2CO↑.C为CO气体;2CO+ O2 2CO2.故F为CO2。因为A、E含元素同周期,而且能与Si反应制取SiO2,则E为O元素;则D的原子结构示意图为;
2CO2.故F为CO2。因为A、E含元素同周期,而且能与Si反应制取SiO2,则E为O元素;则D的原子结构示意图为;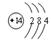 CO2的分子是直线型分子,两个O原子在C原子的两侧,夹角为180?。反应①的化学方程式为C+ SiO2
CO2的分子是直线型分子,两个O原子在C原子的两侧,夹角为180?。反应①的化学方程式为C+ SiO2 Si+2CO↑。(2)若A、D为常见金属单质,且加热时A、D才能溶解在E的浓溶液中,根据金属的活动性顺序可知:A为Fe,D为Cu,E为浓H2SO4。B为CuSO4;反应③的化学方程式为Cu+2H2SO4(浓)
Si+2CO↑。(2)若A、D为常见金属单质,且加热时A、D才能溶解在E的浓溶液中,根据金属的活动性顺序可知:A为Fe,D为Cu,E为浓H2SO4。B为CuSO4;反应③的化学方程式为Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O 。足量的Fe与CuSO4溶液发生反应产生C是FeSO4.F为Fe2(SO4)3.检验Fe2+离子的方法是取少量C溶液于试管中,滴加KSCN溶液无明显颜色变化,再滴加氯水呈血红色。若以惰性电极电解CuSO4的水溶液,电解的方程式为:CuSO4+2H2O
CuSO4+SO2↑+2H2O 。足量的Fe与CuSO4溶液发生反应产生C是FeSO4.F为Fe2(SO4)3.检验Fe2+离子的方法是取少量C溶液于试管中,滴加KSCN溶液无明显颜色变化,再滴加氯水呈血红色。若以惰性电极电解CuSO4的水溶液,电解的方程式为:CuSO4+2H2O  2Cu+2H2SO4+ O2↑。可见当阴极产生2mol的Cu时,阳极产生气体1mol。n(Cu)= 9.6g÷64g/mol=0.15mol,所以n(O2)="0.075mol," V(O2)= n·Vm=" 1.68L." 该反应的离子方程式为:2Cu2+ + 2H2O
2Cu+2H2SO4+ O2↑。可见当阴极产生2mol的Cu时,阳极产生气体1mol。n(Cu)= 9.6g÷64g/mol=0.15mol,所以n(O2)="0.075mol," V(O2)= n·Vm=" 1.68L." 该反应的离子方程式为:2Cu2+ + 2H2O  ?2Cu + O2↑ + 4H+。
?2Cu + O2↑ + 4H+。
本题难度:一般
3、填空题 (8分)X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:①它们的电子层数之和为10;②Z、W元素的原子最外层电子数之和是X元素原子最外层电子数的2倍;③Z和W元素原子质子数之和是X、Y元素原子质子数之和的2倍;④X元素的原子最外层电子数是次外层电子数的2倍。回答下列问题:
(1)X元素为__________,Y元素为____________;
(2)Z元素位于周期表的第________周期;
(3)过量X的最高价氧化物通入氢氧化钠溶液中,小心蒸干,得到固体为:___________;
(4)若Z为钠,则W为?;XYW2的结构式为?,X22-的电子式为?;
(5)写出与XY电子总数相同的一种双原子核微粒的化学式?。
参考答案:(1)C;O(2)三(3)NaHCO3(4)氯;略(5)N2
本题解析:略
本题难度:简单
4、简答题 它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).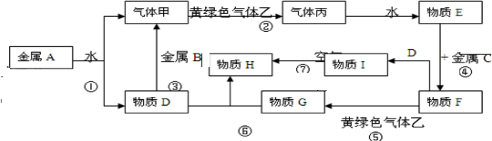
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A______、C______、丙______;
(2)写出反应③的化学方程式______,
写出反应⑤的离子方程式______,
写出反应⑦的化学方程式______;
(3)冶炼金属A、B一般用______法,冶炼金属C一般用______法.
参考答案:黄绿色气体为Cl2,则与Cl2反应的气体甲为H2,丙为HCl,物质E为盐酸,金属A与水反应生成的D可能为碱,也可能为金属氧化物,但D能与金属B反应生成氢气,则D应为碱,为NaOH,所以A为Na,B为Al,盐酸与金属C反应,后还能继续与氯气反应,则金属C为变价金属,应为Fe,所以F为FeCl2,G为FeCl3,I为Fe(OH)2,H为4Fe(OH)3,则
(1)由以上分析可知,A为Na,C为Fe,丙为?HCl,故答案为:Na;Fe;?HCl;
(2)反应③为Al和NaOH溶液的反应,反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,反应⑤为Cl2和FeCl2的反应,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-,Fe(OH)2具有还原性,能与空气中氧气反应生成Fe(OH)3,反应的化学方程式为4Fe(OH)2+2H2O+O2=4Fe(OH)3,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;2Fe2++Cl2=2Fe3++2Cl-;4Fe(OH)2+2H2O+O2=4Fe(OH)3;
(3)Na、Al为活泼金属,应用电解法冶炼,Fe可用热还原法冶炼,故答案为:电解法;?热还原.
本题解析:
本题难度:一般
5、填空题 A、B、C为3种单质(其中A为固体,B、C为气体),将D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色,B、C反应的产物易溶于水得到无色溶液E。它们之间的转化关系如下图: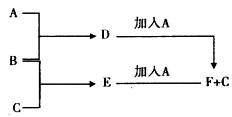
填写下列空白:
(1)物质A是____________,物质B是___________,B元素的离子结构示意图为___________。
(2)写出化合物E的电子式:____________,D的饱和溶液滴入沸水中溶液呈红褐色的原因是(用离子方程式表示):_______________________________,D溶液可以用来止血。
(3)工业上把B单质与石灰乳反应可制得漂白粉,漂白粉的有效成份是_______,漂白粉常用于自来水的杀菌消毒,原因是:(用化学方程式和适当的文字说明)______________________。
(4)F中加入NaOH溶液,并在空气中放置,沉淀由白色变为灰绿色最后变成红褐色的化学方程式是_____________________________________。
参考答案:(1)Fe;Cl2;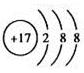
(2)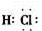 ? FeCl3+3H2O
? FeCl3+3H2O Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
(3)Ca(ClO)2 ;Ca(ClO)2+CO2+H2O=CaCO3+2HClO;次氯酸钙在自来水中与CO2反应后生产了次氯酸,次氯酸有强氧化性,能起杀菌消毒作用(4)4Fe(OH)2+O2+2H2O═4Fe(OH)3
本题解析:A、B、C是三种常见的单质,其中A为固体,B、C为气体;D的饱和溶液滴入沸水中继续煮沸,溶液呈红褐色则D是氯化铁,A、B都是单质,且A是固体,所以A是铁,B是氯气;B和C反应时可观察到苍白色火焰,其产物极易溶于水得无色溶液E,则C是氢气,E是氯化氢,盐酸和铁反应生成氯化亚铁,则F是氯化亚铁。
(1)由上述分析可知,A为Fe,B为Cl2,Cl-的离子结构示意图为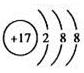 (2)由上述分析知E为HCl,其电子式为
(2)由上述分析知E为HCl,其电子式为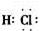 ? D为FeCl3,在沸水中水解生成胶体,该反应为FeCl3+3H2O
? D为FeCl3,在沸水中水解生成胶体,该反应为FeCl3+3H2O Fe(OH)3(胶体)+3HCl(3)B气体制取漂白粉,氯气与石灰乳反应生成氯化钙、次氯酸钙、水,该反应为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,其有效成分为Ca(ClO)2,次氯酸钙在自来水中与CO2反应后生产了次氯酸,次氯酸有强氧化性,能起杀菌消毒作用(4)氯化亚铁和氢氧化钠反应生成白色沉淀氢氧化亚铁,氢氧化亚铁不稳定易被氧气氧化生成红褐色氢氧化铁,反应方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3。
Fe(OH)3(胶体)+3HCl(3)B气体制取漂白粉,氯气与石灰乳反应生成氯化钙、次氯酸钙、水,该反应为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,其有效成分为Ca(ClO)2,次氯酸钙在自来水中与CO2反应后生产了次氯酸,次氯酸有强氧化性,能起杀菌消毒作用(4)氯化亚铁和氢氧化钠反应生成白色沉淀氢氧化亚铁,氢氧化亚铁不稳定易被氧气氧化生成红褐色氢氧化铁,反应方程式为4Fe(OH)2+O2+2H2O═4Fe(OH)3。
本题难度:一般