ʱ��:2020-08-23 07:18:45
1��ѡ���� �����£�ȡ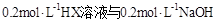 ��Һ�������ϣ����Ի�Ϻ���Һ����ı仯������û����Һ��pH��8��������˵�������ϵʽ����ȷ����
��Һ�������ϣ����Ի�Ϻ���Һ����ı仯������û����Һ��pH��8��������˵�������ϵʽ����ȷ����
A��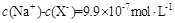
B��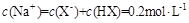
C��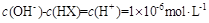
D�������Һ����ˮ�������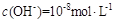
�ο��𰸣�A
�������������Һ��Ϻ�������Һ������ΪNaX������Һ��pH��8��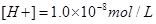 ���ʸ���ҺΪ������Һ����Һ�е������غ�ֱ�Ϊ��
���ʸ���ҺΪ������Һ����Һ�е������غ�ֱ�Ϊ��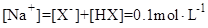 ��
��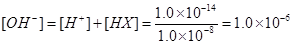 ��
��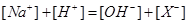 ,��Һ�з�����ˮ��Ϊ
,��Һ�з�����ˮ��Ϊ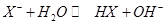 ����ˮ���������
����ˮ���������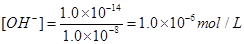 ���ϣ���ѡA��
���ϣ���ѡA��
���������������ۺ��Խ�ǿ�����Ŀ�����ѧ���Ե���غ㡢�����غ㶨�����֪ʶ�����������գ�����Ϊ�߿���Ҫ����֮һ������Ӧ�ö�ע��ƽʱ���ⷽ���֪ʶ���ۡ�
�����Ѷȣ���
2������� ���¸����и����Ĺ�ϵ�����á�������������������ʾ��
��1��pH �� 3�Ĵ����pH��11������������Һ�������ϣ����Һ��c(Na��) ?c(CH3COO��)
��2�������ʵ���Ũ�ȡ����������ʹ����ƻ�ϣ����Һ�и�����Ũ�ȵĴ�С��ϵΪ?
?
��3�������£���NaOH��Һ�е�c(OH��)��NH4Cl��Һ�е�c(H��)��ͬ���ֽ�NaOH��NH4Cl����Һ�ֱ�ϡ��10����ϡ�ͺ�NaOH��NH4Cl��Һ��pH�ֱ���pH1��pH2��ʾ����pH1�� pH2??14
��4������pH��ȡ��������Ba(OH)2��NaOH��NH3��H2O������Һ�������Ƿֱ���V1 L��V2 L��V3 L��Ũ�ȵ������ϣ���Ϻ���Һ�������ԣ���V1 ��V2 ��V3�Ĵ�С��ϵ?
�ο��𰸣���1��c(Na��)��? c(CH3COO��)��2�� c(Cl��)��c(Na��)��c(H��)��c(CH3COO��)��c(OH��)?
��3��pH1�� pH2?��? 14 ��4��V1��V2��V3�Ĵ�С��ϵ? V3�� V1 ��V2
�����������1��pH��ͬ��������ǿ��������ϣ���Һ���������ԣ�c(H��)> c(OH��)���ɵ���غ�֪��������Ũ�ȱ�Ȼ�ǣ�c(Na��)��?c(CH3COO��)
��2�������ʵ���Ũ�ȡ����������ʹ����ƻ�Ϻ��ǵ�Ũ�ȵ�NaCl��CH3COOH��Һ��NaClȫ�����룬CH3COOH���ֵ��룬��Һ�����ԡ�
����c(Cl��)��c(Na��)��c(H��)��c(CH3COO��)��c(OH��)
��3�������ü��跨��ֱ�ӡ�����NaOH��Һ��pHΪ11��NH4Cl��Һ��pH��Ϊ3��
���ͬʱϡ��10������NaOH��Һ��pHΪ12����NH4Cl��Һ������ˮ��ƽ��Ĵ��ڣ���pH�����С��4����pH1�� pH2?��?14
(4)��ǿ����Һ��OH��Ũ����ͬ����Ȼ������ͬ���ᣬ��V1 ��V2��?������������е���ƽ�⣬��ȻҪ���ĸ�����ᣬ����V3�� V1 ��V2
�����Ѷȣ�һ��
3������� ���г����µ�0.1 mol/l������Һ��
��1������Һ�ʼ�������Ϊ����ˮ��ƽ�⣬������ӷ���ʽ�ǣ�________________��Ϊ֤����������ƽ�⣬��������ʵ�飺��0.1 mol��l��1������Һ�еμӷ�̪����Һ�Ժ�ɫ��������Һ�еμ�?���ѧʽ����Һ����ɫ����Ϊ��ɫ��˵�������۵������
��2��ͬѧ�ײ������ϵ�֪0.1 mol/LNa2CO3�У�����ˮ���CO32����������������10%�������ʵ�����֤����д��ʵ�鷽����Ԥ�ڹ۲쵽����������?��
��3��ͬѧ�Ҿ���Һ������Ũ�ȹ�ϵд�������ϵʽ�����в���ȷ����?��
A��c(Na��)��2c(CO32��)
B��c(CO32��)��c(OH��)��c(HCO3��)��c(H2CO3)
C��c(OH��)��c(H��)��c(HCO3��)��2c(H2CO3)
D��c(CO32��)��c(HCO3��)="0.1" mol��L��1
E��c(H��)+ c(Na��)�� c(OH��)��c(HCO3��)��c(CO32��)
��4��������pH��Ϊa��Na2CO3��NaOH��Һ�У�ˮ���������c(OH��)֮��=?��
�ο��𰸣���1��CO32- + H2O HCO3- + OH-? BaCl2��CaCl2
HCO3- + OH-? BaCl2��CaCl2
��2����0.1 mol��L-1Na2CO3��ҺpH��pH��12?��3��D��E?��4��10(2a-14)
���������(1) ����̼������ǿ�������Ρ�����Һ�д��ڵ�ˮ��ƽ����Ҫ��CO32- + H2O HCO3- + OH-������HCO3- + H2O
HCO3- + OH-������HCO3- + H2O H2CO3-+ OH-������������ˮ���������H+����������ʹ��Һ�е�c(OH-)��c(H+)�������Һ�Լ��ԡ�������Һ�еμ���CO32-�γɳ�����������BaCl2��CaCl2����ʱ��ų�������Ӧ��������CO32-��c(CO32-)��С������ˮ��̶������ǵ�λ����е�OH-�����ʵ������٣�������Һ�ļ��Լ�������ɫ����Ϊ��ɫ��(2)��Na2CO3��Һ����Ҫ����ˮ��ƽ��CO32- + H2O
H2CO3-+ OH-������������ˮ���������H+����������ʹ��Һ�е�c(OH-)��c(H+)�������Һ�Լ��ԡ�������Һ�еμ���CO32-�γɳ�����������BaCl2��CaCl2����ʱ��ų�������Ӧ��������CO32-��c(CO32-)��С������ˮ��̶������ǵ�λ����е�OH-�����ʵ������٣�������Һ�ļ��Լ�������ɫ����Ϊ��ɫ��(2)��Na2CO3��Һ����Ҫ����ˮ��ƽ��CO32- + H2O HCO3- + OH-��c(CO32-)(ʼ)=" 0.1" mol/L������ˮ��̶ȵ���10%������ˮ�ⷽ��ʽ��֪��c(OH-)=0.01mol/L��c(H��)=10-12mol/L.pH=12.ˮ��̶�Խ��ˮ�������c(OH-)��Խ�ߣ���Һ��pH��Խ����ˮ��̶�С��10%����c(H��)��10-12mol/L.pH<12����ˣ���0.1 mol��L-1Na2CO3��ҺpH����pH��12��֤��0.1 mol/LNa2CO3�У�����ˮ���CO32����������������10%����3��A���������غ�ɵ�c(Na��)=2c(CO32��)+2 c(HCO3��)+2c(H2CO3).����c(Na��)��2c(CO32��) ����ȷ��B����Na2CO3�д���ˮ��ƽ�⣺CO32- + H2O
HCO3- + OH-��c(CO32-)(ʼ)=" 0.1" mol/L������ˮ��̶ȵ���10%������ˮ�ⷽ��ʽ��֪��c(OH-)=0.01mol/L��c(H��)=10-12mol/L.pH=12.ˮ��̶�Խ��ˮ�������c(OH-)��Խ�ߣ���Һ��pH��Խ����ˮ��̶�С��10%����c(H��)��10-12mol/L.pH<12����ˣ���0.1 mol��L-1Na2CO3��ҺpH����pH��12��֤��0.1 mol/LNa2CO3�У�����ˮ���CO32����������������10%����3��A���������غ�ɵ�c(Na��)=2c(CO32��)+2 c(HCO3��)+2c(H2CO3).����c(Na��)��2c(CO32��) ����ȷ��B����Na2CO3�д���ˮ��ƽ�⣺CO32- + H2O HCO3- + OH-�� HCO3- + H2O
HCO3- + OH-�� HCO3- + H2O H2CO3-+ OH-����Ҫ�ǵ�һ��ˮ�⣬����c(HCO3��)�� c(H2CO3)��������ˮ��ij̶��Ǻ����ģ��εĵ������ô���ˮ�����ã�����c(CO32��)�� ��c(HCO3��)����������ˮ�ⶼ����OH����HCO3����һ��ˮ����������ڵڶ���ˮ���������ġ�����c(OH��)��c(HCO3��)���������Һ�����Ӽ�Ĺ�ϵΪ�� c(CO32��)��c(OH��)��c(HCO3��)��c(H2CO3)����ȷ��C����Һ�Լ��ԡ����������غ�ɵã�c(OH��)��c(H��)��c(HCO3��)��2c(H2CO3)����ȷ��D�����������غ�ɵ�c(CO32��)��c(HCO3��)+ c(H2CO3)="0.1" mol/L.����E�����ݵ���غ�ɵ�c(H��)+ c(Na��)�� c(OH��)��c(HCO3��)��2c(CO32��).����4��������pH��Ϊa��Na2CO3��Һ��c(H��)=10-a, c(OH��)(ˮ)=10-14��10-a =10a-14mol/L.����pH=a��NaOH��Һc(H��)(ˮ)= c(OH��)(ˮ)=10-amol/L.����ˮ���������c(OH��)֮��=10a-14��10-a=10(2a-14)��
H2CO3-+ OH-����Ҫ�ǵ�һ��ˮ�⣬����c(HCO3��)�� c(H2CO3)��������ˮ��ij̶��Ǻ����ģ��εĵ������ô���ˮ�����ã�����c(CO32��)�� ��c(HCO3��)����������ˮ�ⶼ����OH����HCO3����һ��ˮ����������ڵڶ���ˮ���������ġ�����c(OH��)��c(HCO3��)���������Һ�����Ӽ�Ĺ�ϵΪ�� c(CO32��)��c(OH��)��c(HCO3��)��c(H2CO3)����ȷ��C����Һ�Լ��ԡ����������غ�ɵã�c(OH��)��c(H��)��c(HCO3��)��2c(H2CO3)����ȷ��D�����������غ�ɵ�c(CO32��)��c(HCO3��)+ c(H2CO3)="0.1" mol/L.����E�����ݵ���غ�ɵ�c(H��)+ c(Na��)�� c(OH��)��c(HCO3��)��2c(CO32��).����4��������pH��Ϊa��Na2CO3��Һ��c(H��)=10-a, c(OH��)(ˮ)=10-14��10-a =10a-14mol/L.����pH=a��NaOH��Һc(H��)(ˮ)= c(OH��)(ˮ)=10-amol/L.����ˮ���������c(OH��)֮��=10a-14��10-a=10(2a-14)��
�����Ѷȣ�һ��
4��ѡ���� ����ʱ����10mL�Ĵ���ϡ��Һ����ε���NaOHϡ��Һ���������й�������ȷ����
A��ʵ�������ˮ�ĵ���̶ȵı仯����������С
B������Һ������ʱ����Ӧǡ����ȫ
C������Ӧǡ����ȫʱ������NaOH��Һ10mL
D������Һ�ʼ���ʱ����������Ũ���ɴ�С��˳�����Ϊc(Na+)>c(OH-)>c(Ac-)>c(H+)
�ο��𰸣�AD
����������ڷ�Ӧ�����ɴ����ƣ�������ˮ��ٽ�ˮ�ĵ��롣����Ӧ�������ټ�����������������ˮ�ĵ��룬A��ȷ��ǡ�÷�Ӧʱ���ɴ����ƣ�������ˮ���Լ��ԣ�B����ȷ�������Ũ����ȷ�������Բ��ܼ����������Ƶ�Ũ�Ⱥ������C����ȷ�����ݵ���غ�c(Na+)��c(H+)��c(OH-)��c(Ac-)��֪��ѡ��D��ȷ����ѡAD��
�����Ѷȣ�һ��
5��ѡ���� ��֪��t�棬ijBa(OH)2ϡ��Һ�У�c(H��) = 10-a mol��L��1��c(OH��) = 10-b mol��L��1����a+b=16�������Һ����μ���pH = c�����ᣬt���²�û��Һ��pH����ͼ��ʾ
| ��� | Ba(OH)2��Һ���/mL | �������/mL | ���ҺpH |
| 1 | 22.00 | 0 | 10 |
| 2 | 22.00 | 18.00 | 9 |
| 3 | 22.00 | 22.00 | 8 |
�ο��𰸣�D
����������������֪���¶���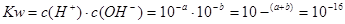 ��������Һ��PH=8ʱ������ҺΪ���ԣ����ԣ����ɵ������������c=6��
��������Һ��PH=8ʱ������ҺΪ���ԣ����ԣ����ɵ������������c=6��
�����Ѷȣ�һ��