ʱ��:2020-08-23 06:59:33
1������� ��NaOH��������250mL0.1?mol��L-1��Һ�����У�����NaOH����______g? ���ƹ�����������������������ʹ��Һ���ʵ���Ũ����α仯�����ƫ�ߡ�����ƫ�͡����䡱��
��?����NaOH�ѳ��⣬����___________��?
��?ת��ʱδϴ���ձ�������___________��
��?��������ƿδ�������___________��?
��?����ʱ���ӣ�����____________��
��?����ʱ�����ҩƷ�ŷ��ˣ�5������ʹ�����룩������____________��
�ο��𰸣�1?�� ��1��ƫ�� ����2��ƫ�� ����3����Ӱ�� ����4��ƫ�� ����5��ƫ��
���������
�����Ѷȣ�һ��
2������� ʵ����ʹ�õ�Ũ�����������������һ��Ϊ36.5%���ܶ�1.19g/cm3��
��1����______���Ȼ��⣨��״����ͨ��1.00Lˮ�п��Եõ�36.5%��Ũ���
��2����Ũ��������ʵ���Ũ��Ϊ______��
�ο��𰸣���1������Ҫ�Ȼ�������ΪVL����HCl�����ʵ���ΪVL22.4L/mol=V22.4mol����HCl������ΪV22.4mol��36.5g/mol=36.5V22.4g��1.00Lˮ������Ϊ1L��1000g/L=1000g������Һ������Ϊ��1000+36.5V22.4��g���ʣ�1000+36.5V22.4��g��36.5%=36.5V22.4g����ã�V=352.8L��
�ʴ�Ϊ��352.8��
��2����������Ϊ36.5%���ܶ�1.19g/cm3��Ũ��������ʵ���Ũ��Ϊ1000��1.19��36.5%36.5mol/L=11.9mol/L��
�𣺸�Ũ��������ʵ���Ũ��Ϊ11.9mol/L��
���������
�����Ѷȣ�һ��
3������� ����ڿ�ѧ����������������Ҫ��Ӧ�á�ʯ��ϼ���һ�ֺܺõ�ֲ��ɱ��������������ʯ�ҡ�ˮ�ȷ�Ӧ���èD�D�ɶ���[ CaSx��x��5��]������������ɵĻ�����ͬ������ʯ�Һ������ˮ��Һ�з�Ӧ�������ɲ�ͬ�Ķ��ƺ��������ơ��磺
3Ca(OH)2+8S 2CaS3+CaS2O3+3H2O��
2CaS3+CaS2O3+3H2O��
3Ca(OH)2+6S 2CaS2+CaS2O3+3H2O�ȡ�
2CaS2+CaS2O3+3H2O�ȡ�
��������������м��㣺
��1��������ܽ���������Һ������һ�ֶ�����ö���������Ԫ�ص���������Ϊ0.736��ͨ������ȷ��Na2Sx��x=?��
��2����ȡijʯ��ϼ�������ֻ�����ֺ����250mL���ܶ�Ϊ1.12g/mL��ͨ������CO2ʹ����ٷֽ⡣ԭ�����£�
Sx2-+2H2O+2CO2��(x-1)S��+H2S��+ 2HCO3-��S2O32- + H2O+CO2��HSO3-+HCO3-+S�� ��
��ȫ��Ӧ���ռ�������1.12����S��P��T����������������Һ�е��ܽ⣩�����ʯ��ϼ��ж��Ƶ����ʵ���Ũ��Ϊ?���������Ƶ���������Ϊ?��������С����ʾ������2λ��Ч���֣�
��3�����������ʯ�ҡ���Ǻ�ˮ��������7��16��70�������ȫ��Ӧ��ֻ�������ֺ���Ļ�������ʯ��ϼ��ж������������Ƶ����ʵ���֮����?�����ƵĻ�ѧʽ��?��
��4����������ʯ��50.4g�����96g��ˮ504gǡ����ȫ��Ӧ�������ֶ��ƣ�������CaS4֮��ж��ֶ��ơ�����������ֶ��ƿ��ܵ����ʵ���֮�ȣ�д��������̣���
�ο��𰸣���1����4?��2�֣�?��2����0.20 mol/L ��2�֣�? 0.014?��2�֣�
��3����2:1?��2�֣�? CaS5?��2�֣�
��4����n(CaO)="50.4/56" =0.3mol? n(S)="96/32" =3mol?��1�֣�?
�� n[Ca(OH)2 ]: n(S) =" 3" : 10?�ɷ�Ӧ��֪��3Ca(OH)2+10S 2CaSx+CaS2O3+3H2O
2CaSx+CaS2O3+3H2O
��֮�ã�x="4" ������������ԭ�ӵ�ƽ��ֵΪ4��?��1�֣�
�������ֶ��������Ϊ��CaS2��CaS5��CaS3��CaS5��?��2�֣�
��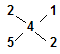 ?��֪��n(CaS2)��n(CaS5)=1:2����1�֣�
?��֪��n(CaS2)��n(CaS5)=1:2����1�֣�
��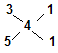 ?��֪��n(CaS3)��n(CaS5)=1:1?��1�֣�
?��֪��n(CaS3)��n(CaS5)=1:1?��1�֣�
���������ⷨҲ���Ը��֡�
�����������1��. ��Ԫ�ص���������Ϊ0.736������Ԫ�ص���������Ϊ0.264��������ԭ�Ӻ���ԭ�ӵĸ���֮����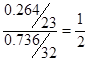 ������x��4.
������x��4.
��2��������0.05mol�����Ը��ݷ���ʽ��֪�����Ƶ����ʵ�����0.05mol����Ũ����0.05mol��0.25L��0.20 mol/L������+CaS2O3�����ʵ�����0.05mol��2��0.025mol������������������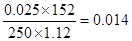 ��
��
��3����ʯ�ҡ���ǵ�������7��16�������ʵ���֮����1�U4�����������ƺ���ǵ����ʵ���֮����1�U4�����Է���ʽΪ3Ca(OH)2+12S 2CaSx+CaS2O3+3H2O�����x��5��
2CaSx+CaS2O3+3H2O�����x��5��
��4��n(CaO)="50.4/56" =0.3mol? n(S)="96/32" ="3mol"
�� n[Ca(OH)2 ]: n(S) =" 3" : 10?�ɷ�Ӧ��֪��3Ca(OH)2+10S 2CaSx+CaS2O3+3H2O
2CaSx+CaS2O3+3H2O
��֮�ã�x="4" ������������ԭ�ӵ�ƽ��ֵΪ4��
�������ֶ��������Ϊ��CaS2��CaS5��CaS3��CaS5��
�� ��֪��n(CaS2)��n(CaS5)=1:2��
��֪��n(CaS2)��n(CaS5)=1:2��
�� ��֪��n(CaS3)��n(CaS5)=1:1
��֪��n(CaS3)��n(CaS5)=1:1
�����Ѷȣ�һ��
4������� ��3.22gâ����Na2SO4��10H2O������ˮ�У�Ҫʹÿ100��ˮ����������1��Na+������ˮ������Ϊ?g��
�ο��𰸣�34.2
���������3.22gâ�������ʵ���Ϊ3.22g/322(g/mol) =0.01mol
������Һ��n��Na+��=2n��Na2SO4?10H2O��=0.01mol��2=0.02mol
ÿ100��ˮ����������1�������ӣ�����n��H2O��=100n��Na+��=2mol
0.01molNa2SO4?10H2O�к���ˮ�����ʵ���Ϊ0.01mol��10=0.1mol
������Ҫ��ˮ�����ʵ���Ϊ2mol-0.1mol=1.9mol
������Ҫˮ������Ϊ1.9mol��18g/mol=34.2g
����Ҫˮ������Ϊ34.2g��
�������������ʵ������й�Ũ�ȼ��㣬�Ѷ��еȣ���ȷˮ���ܵ�����ȥNa2SO4?10H2O�����к���ˮ����Ϊ��Ҫ�����ˮ�ǽ���ؼ���
�����Ѷȣ�һ��
5��ѡ���� �����ӵ�����ԼΪ6.02��1023mol��1��������������ȷ����
�ţ�0.25molNa2O2�к��е���������Ϊ0.5��6.02��1023?�ƣ�7.5gSiO2�����к��еĹ�������Ϊ0.5��6.02��1023?�ǣ�2.24LCH4�к��е�ԭ����Ϊ0.5��6.02��1023
�ȣ�250mL2mol/L�İ�ˮ�к���NH3��H2O�ķ�����Ϊ0.5��6.02��1023?�ɣ�1L 1mol��L�D1��HAc��Һ�к���6.02��1023��������?�ʣ�18g D2O����ˮ����ȫ��⣬ת��
6.02��1023������?�ˣ�22.4L SO2���壬������ԭ����Ϊ2��6.02��1023
�̣�14g��ϩ�ͱ�ϩ�Ļ�����У����й��õ��Ӷ���ĿΪ3��6.02��1023
A��2��
B��3��
C��5��
D��6��
�ο��𰸣�A
����������Ŵ�����Ϊ0.25molNa2O2�к��е�������0.25moL;����ȷ��n(SiO2)="7.5/60" mol=0.125mol,ÿĦ��SiO2���й��ۼ��ǣ�1��4+2��2��/2 moL=4mol, 7.5gSiO2�����к��еĹ�������Ϊ0.125��4��6.02��1023=0.5��6.02��1023 ;�Ǵ�����֪������Ĵ��ڵ������������㣻�ȴ�����Ϊ��ˮ�д���������ƽ��NH3 + H2O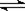 NH3��H2O
NH3��H2O 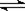 ?NH4++OH-? ;�ɴ�����ΪHac��������ʡ��ʴ���18g D2O�����ʵ���С��1mol���˴�����Ϊ��֪������Ĵ�������������ȷ����Ϊ��ϩ���ϩ�����ʽ����CH2��1.4g��ϩ���ϩ�Ļ�������൱�ں���0.1molCH2��
?NH4++OH-? ;�ɴ�����ΪHac��������ʡ��ʴ���18g D2O�����ʵ���С��1mol���˴�����Ϊ��֪������Ĵ�������������ȷ����Ϊ��ϩ���ϩ�����ʽ����CH2��1.4g��ϩ���ϩ�Ļ�������൱�ں���0.1molCH2��
�����Ѷȣ�һ��