时间:2020-08-23 06:55:42
1、实验题 (9分)酸碱中和滴定是中学化学常见实验。
某同学欲测定某浓硫酸样品的物质的量浓度,进行了以下实验操作:
A.冷却至室温后,在100mL容量瓶中定容配成100mL稀硫酸。
B.量取20.00mL稀硫酸于锥形瓶中并滴入几滴指示剂。
C.将酸式滴定管和碱式滴定管用蒸馏水洗涤干净,并用各待盛溶液润洗。
D.将物质的量浓度为1.50mol/L标准NaOH溶液装入碱式滴定管,调节液面记下读数V1。
E.继续滴定至终点,记下读数为V2。
F.在锥形瓶下垫一张白纸,把锥形瓶移到碱式滴定管下小心滴入NaOH标准溶液,边滴边摇动锥形瓶。
G.量取浓硫酸样品5mL,在烧杯中用蒸馏水溶解。
H.重复以上实验。
请回答下列问题:
(1)该实验正确操作步骤的顺序为:
→ A→ →  →D→ → → H
→D→ → → H
(用编号字母填写)。
(2)量取5mL浓硫酸的仪器是 ;量取20.00mL稀硫酸的仪器是 。
(3)选用的指示剂是 。滴定过程中,视线应注视 ;判断到达滴定终点的现象是 。
(4)下表是实验测得的有关数据:
| 滴定序号 | 待测稀硫酸的体积(mL) | 所消耗NaOH标准溶液液的体积(mL) | |
| V1 | V2 | ||
| ① | 20.00 | 0.50 | 22.60 |
| ② | 20.00 | 6.00 | 27.90 |
参考答案:
本题解析:略
本题难度:一般
2、选择题 已知下列热化学方程式:(l) C(s)+1/2O2(g)=CO(g)?△H =△H1
(2)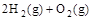 ?=2H2O(g)?△H=△H2
?=2H2O(g)?△H=△H2
由此可知 C(s)+ H2O(g) ==?CO(g) + H2(g)?ΔH3。则?ΔH3等于? (? )
A.△H1-△H2
B.△H1-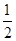 △H2
△H2
C.2△H1-△H2
D.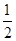 △H2 -△H1
△H2 -△H1
参考答案:B
本题解析:(l)―(2)*1/2 即得C(s)+ H2O(g) ==?CO(g) + H2(g) ,所以ΔH3=△H1-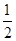 △H2
△H2
本题难度:简单
3、选择题 313 K时,水的KW=3.0×10-14,则在313 K时,c(H+)=10-7 mol/L的溶液(?)
A.呈酸性
B.呈中性
C.呈碱性
D.无法判断
参考答案:C
本题解析:解答本题时应注意以下两点:
(1)判断溶液的酸碱性最根本的依据是溶液中c(H+)与c(OH-)的相对大小;
(2)根据水在一定温度下的KW可以通过计算确定溶液呈中性时的c(H+)。
本题难度:一般
4、选择题 等浓度的下列物质的水溶液,加热到80℃,忽略水的蒸发,溶液的pH不变的是(?)?
A.Na2CO3
B.NaOH
C.Na2SO4
D.H2SO4
参考答案:D
本题解析:略
本题难度:一般
5、填空题 (10分)现在城市居民使用的管道煤气的主要成分是H2、CO和少量CH4。H2、CO和CH4的燃烧热数据如下表
| 物质 | H2 | CO | CH4 |
| 燃烧热kJ?mol-1 | 285.8 | 283.0 | 890.3 |
参考答案:(1) H2(g)+1/2O2(g)=H2O(l) ΔH3=-285.8KJ/mol;CO(g)+ 1/2O2(g)= CO2(g) ΔH=-283.0KJ/mol ;CH4(g)+2O2(g)= CO2(g)+2H2O(l) ΔH=-890.3KJ/mol ;(2)空气、天然气;0.44.
本题解析:(1)根据表格中物质的燃烧热的数值可知:H2、CO和CH4燃烧的热化学方程式是(1) H2(g)+1/2O2(g)=H2O(l) ΔH3=-285.8KJ/mol;CO(g)+ 1/2O2(g)= CO2(g) ΔH=-283.0KJ/mo l ;CH4(g)+2O2(g)= CO2(g)+2H2O(l) ΔH=-890.3KJ/mol ;(2)作为开发西部的西气东输工程的重要成就,西部天然气已全面进入上海、江苏境内,使用管道煤气用户改用天然气,由于单位体积的天然气消耗的氧气量大,所以应调整灶具进气量阀门,即增大空气的进入量或减少天然气的进入量。据报道,同时燃气价格也将在现有的0.95元/m3的基础上调整到1.31元/m3,由于1mol的管道煤气燃烧放出热量是(283.0+285.8)KJ÷2=284.4KJ;1mol的天然气放出热量是890.3KJ,所以若居民保持生活水平不变,即消耗的能量不变,因此需要消耗天然气的物质的量的煤气的284.4KJ÷890.3KJ=0.32倍,原来消耗1m3,花费0.95元,则消耗的天然气的体积是0.32m3,需要花费:0.32m3×1.31元/m3=0.42元,所以在消耗燃气方面的消费大约是现在的倍数关系是:0.42元÷0.95元=0.44(倍),故更经济。
考点:考查燃烧热的热化学方程式的书写、燃烧不同燃料的灶具的改造方法、花费大小的比较的计算。
本题难度:一般